题目内容
17.某含铁盐是一种绿色、无污染的净水剂,其化学式为Na2FeO4,则其中铁元素的化合价是( )| A. | +2 | B. | +3 | C. | +4 | D. | +6 |
分析 根据在化合物中正负化合价代数和为零,结合Na2FeO4的化学式进行解答即可.
解答 解:钠元素显+1价,氧元素显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
故选:D.
点评 本题难度不大,掌握利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答此类题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列化学用语表达正确的是( )
| A. | 复合肥料磷酸二氢铵的化学式:(NH4)2HPO4 | |
| B. | 碳原子的结构示意图: | |
| C. | 在人体组织里葡萄糖的转化:C6H12O6+9O2 $\frac{\underline{\;酶\;}}{\;}$ 6 CO2+6 H2O | |
| D. | 过氧化氢中氢、氧元素的化合价:$\stackrel{+1}{{H}_{2}}$$\stackrel{-1}{{O}_{2}}$ |
12.欲将含有盐酸的CaCl2溶液中和至中性而不引入新的杂质,在没有指示剂的情况下,应加入的试剂是( )
| A. | 石灰石粉末 | B. | 生石灰 | C. | 熟石灰 | D. | 纯碱 |
9.下列说法错误的是( )
| A. | 用灼烧的方法能区别棉花和羊毛 | |
| B. | 用pH试纸能区分肥皂水和石灰水 | |
| C. | 用适量的水能区分NH4NO3固体和NaOH固体 | |
| D. | 用饱和CuSO4溶液能区分食盐水和蛋白质溶液 |
6.水是重要的自然资源,下列“水”中属于纯净物的是( )
| A. | 雨水 | B. | 矿泉水 | C. | 石灰水 | D. | 蒸馏水 |
 的粒子符号Al3+;
的粒子符号Al3+; 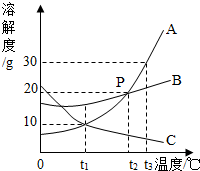 如图为A、B、C三种固体物质的溶解度曲线,请根据图示回答下列问题:
如图为A、B、C三种固体物质的溶解度曲线,请根据图示回答下列问题: