题目内容
一定质量的锌、铁分别和等量的盐酸反应,产生氢气质量与时间的关系如图所示,下列说法不正确的是( )

|
| A. | t1时,产生氢气的质量锌比铁大 | B. | t1时,产生氢气的速率锌比铁大 |
|
| C. | t2时,参加反应锌的质量与铁相同 | D. | t2时,锌、铁消耗的盐酸质量相同 |
| 金属的化学性质.. | |
| 专题: | 压轴实验题;金属与金属材料. |
| 分析: | A、根据图象.比较t1时,锌、铁与盐酸产生氢气质量的多少; B、根据图象.比较t1时,锌、铁与盐酸产生氢气速率的大小; C、根据图象比较t2时,参加反应的锌、铁质量; D、根据图象比较t2时,参加反应的盐酸的质量. |
| 解答: | 解:A、由图象可知,t1时,产生氢气的质量锌比铁大.故A正确; B、t1时,产生氢气的质量锌比铁大.所以,产生氢气的速率锌比铁大.故B正确; C、t2时,生成的氢气的质量相同,根据Zn~H2和Fe~H2,可知65gZn生成2g氢气,56gFe生成2g氢气,因此参加反应锌的质量与铁不同,故C不正确; D、t2时,生成的氢气的质量相同,锌、铁消耗的盐酸质量相同.故D正确. 故选C. |
| 点评: | 活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;相同质量酸与足量金属反应生成氢气的质量相同,据此结合图象细心分析解答. |

2011年3月11日,震惊全球的日本地震造成福岛核电站毁坏,致使放射性碘泄漏,造成了严重的核污染.这里的碘是指( )
|
| A. | 碘离子 | B. | 碘原子 | C. | 碘元素 | D. | 碘分子 |
有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入等质量等浓度的稀硫酸中,乙、丙表面有气泡产生,且丙产生气泡较快;再将甲投入丁的盐溶液中,甲的表面有丁析出,则这四种金属活动性顺序为( )
|
| A. | 甲>乙>丙>丁 | B. | 丙>乙>甲>丁 | C. | 丙>乙>丁>甲 | D. | 丁>甲>乙>丙 |
某研究性学习小组为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用下表中的不同试剂进行实验.下列选项错误的是( )
| 选项 | 所用试剂 | 现象和结论 |
| A | 硫酸铜溶液 | 出现蓝色沉淀,则氢氧化钠过量 |
| B | 石蕊溶液 | 呈紫色,则恰好完全反应 |
| C | 锌粒 | 有气泡产生,则硫酸过量 |
| D | 氯化钡溶液 | 出现白色沉淀,则硫酸过量溶液 |
|
| A. | A | B. | B | C. | C | D. | D |
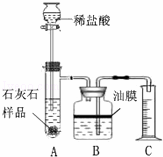
某科学兴趣小组同学为测定一种石灰石中碳酸钙的质量分数,组装了如图的实验装置进行实验.称取质量为1.2克的石灰石样品,将其与足量的稀盐酸反应,每隔10秒读出量筒中水的体积,得到的相关数据(见表格).请根据数据回答下列问题:
| 反应时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
| 量筒中水的体积/ml | 70 | 125 | 170 | 205 | 220 | 220 |
(1)实验装置B中油膜的作用是 .
(2)根据图中的数据,分析该反应速率如何变化并说明原因: .
(3)该样品中碳酸钙的质量分数是多少?(标准状况下二氧化碳的密度是2克/升,计算结果保留一位小数)
 验事实可以用
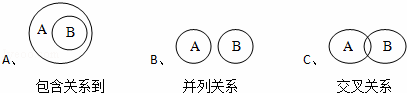
验事实可以用 SO4、CuSO4溶液都能使蛋白质出现白色沉淀
SO4、CuSO4溶液都能使蛋白质出现白色沉淀