题目内容
2.下列说法正确的是( )| A. | 100mL溶质质量分数为40%(密度为1.3g/mL)的硫酸溶液中含硫酸的质量为40g | |
| B. | 30℃时,100g饱和KCl溶液中含 27gKCl,则30C,KCl的溶解度不等于27g | |
| C. | 30℃时100g水中最多溶解37gKCl,则30gKCl饱和溶液中溶质的质量分数为37% | |
| D. | 20℃时硝酸钾溶液的质量分数为5%,可理解为100g硝酸钾溶液中含硝酸钾5g |
分析 A、根据溶质的质量=溶液的质量×溶质质量分数进行分析;
B、根据溶解度的概念进行分析;
C、根据溶质质量分数的计算方法进行分析;
D、根据溶质质量分数的定义进行分析.
解答 解:A、100mL溶质质量分数为40%(密度为1.3g/mL)的硫酸溶液中含硫酸的质量为100mL×1.3g/mL×40%=52g≠40g,故A错误;
B、在一定温度下,某物质在100g溶剂里达到饱和时溶解的质量称为该物质的溶解度,所以30℃时,100g饱和KCl溶液中含27gKCl,则30C,KCl的溶解度不等于27g,故B正确;
C、30℃时100g水中最多溶解37gKCl,则30gKCl饱和溶液中溶质的质量分数为$\frac{37g}{137g}$×100%=27%,故C错误;
D、20℃时硝酸钾溶液的质量分数为5%,可理解为100g硝酸钾溶液中含硝酸钾5g,故D正确.
故选:BD.
点评 本题主要考查了溶质质量分数的计算,难度不大,注意结合定义进行认真分析即可完成.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
19.某同学为测定10g某赤铁矿石中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:氢气也有一氧化碳相似的化学性质3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O;杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:得到数据如表:
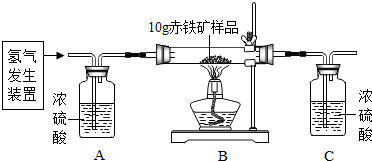
(1)实验前先通一会氢气原因排出装置内的空气,防止加热时产生爆炸;试验中观察到的实验现象为红色粉末变黑;实验结束时先停止加热后停止通入氢气,原因防止生成的铁被氧化.
(2)请计算该赤铁矿石样品中氧化铁的质量分数.80%
(3)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为[(296.8g-294.1g)-(84.3g-81.9g)]:(84.3g-81.9g)(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会不变(选填“偏大”、“偏小”或“不变”).

| 装置 | B | C |
| 反应前质量 | 84.3g | 294.1g |
| 反应后质量 | 81.9g | 296.8g |
(2)请计算该赤铁矿石样品中氧化铁的质量分数.80%
(3)该实验还可测定组成水中各元素之间的质量关系,请用表中实验数据列式表示出水中氢、氧元素的质量比为[(296.8g-294.1g)-(84.3g-81.9g)]:(84.3g-81.9g)(只列式,不计算);若玻璃管中的氧化铁没有完全反应,则求得水中氢、氧元素的质量比会不变(选填“偏大”、“偏小”或“不变”).
10.A、B、C、D四种物质各10克,放入密闭容器中,一定条件下充分反应后,称量,A为12克,B的质量未知,C为6克,D的质量大于10克,则关于A、B、C、D的说法正确的是( )
| A. | A、B是反应物,C、D是生成物 | |
| B. | B可能是催化剂,A、D一定是生成物 | |
| C. | 反应过程中,当容器中C的质量为8克时,D的质量为6克 | |
| D. | 反应结束后经检验B不存在,则容器中D的质量为22克 |
14.由Mg、Fe、CuO组成的混合物加入适量的盐酸,充分反应后铁有剩余,则该溶液中含有的金属阳离子是( )
| A. | Mg2+和Fe2+ | B. | Mg2+ Fe2+和Cu2+ | C. | Mg2+和Cu2+ | D. | Fe2+和Cu2+ |
11.纳米材料被誉为21世纪最有前途的新型材料,许多材料达到纳米(1纳米=10-9米)级的大小时,会产生许多让你料想不到的、奇特的光、电、磁、热、力和化学等方面的性质.如:将金属制成纳米粉末后就变成了黑色,且不导电,机械强度也大幅度提高.由此你判断下列说法错误的是( )
| A. | 纳米碳质地很柔软,构成其的基本粒子是碳原子 | |
| B. | 纳米氧化锌能吸收电磁波 | |
| C. | 黑色的氧化铜粉末属于纳米材料 | |
| D. | 若将银白色铁通过特殊加工成纳米粉末,其物理性质将发生一定的变化 |
12.下列说法中,正确的是( )
| A. | 实验室制氧气必须用二氧化锰做催化剂 | |
| B. | 工业上采用分离液态空气法制氧气,该过程属于分解反应 | |
| C. | 化学反应前后,催化剂的质量和性质都保持不变 | |
| D. | 当混有高锰酸钾的氯酸钾时,氯酸钾的分解速率会加快 |
 锌与稀硫酸反应时加入少量的硫酸铜可以加快产生氢气的速率,等质量的两份锌,向其中加入等质量等浓度且过量的稀硫酸,并向其中一份中加几滴硫酸铜溶液,产生氢气的质量随时间变化图象如图所示.
锌与稀硫酸反应时加入少量的硫酸铜可以加快产生氢气的速率,等质量的两份锌,向其中加入等质量等浓度且过量的稀硫酸,并向其中一份中加几滴硫酸铜溶液,产生氢气的质量随时间变化图象如图所示. 小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待的做起了这个实验:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,
小兵在一本参考书上发现,镁居然能在二氧化碳气体中燃烧!于是他迫不及待的做起了这个实验:将镁条点燃后迅速伸入盛有二氧化碳的集气瓶中,发现镁条剧烈燃烧,发出白光,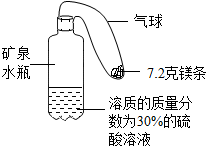 某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.
某实验小组同学设计了如图装置模拟氢气探空气球(装置中气球固定在矿泉水瓶上).将气球中的镁条加入到硫酸溶液中,恰好完全反应.