题目内容
15. 2012年4月15日,央视《每周质量报告》对“非法厂商用皮革下脚料造药用胶囊”曝光,其制成的胶囊往往重金属铬超标.
2012年4月15日,央视《每周质量报告》对“非法厂商用皮革下脚料造药用胶囊”曝光,其制成的胶囊往往重金属铬超标.(1)“铬中毒”中的铬是指铬元素(填“分子”或“原子”或“单质”或“元素”);误食重金属盐后,可尽快喝适量牛奶或鸡蛋清解毒.牛奶和鸡蛋清富含的营养素是C(填字母).
A.糖类 B.油脂 C.蛋白质 D.维生素
(2)如图是铬元素在周期表中的一格,从该图中可知铬元素的核电荷数为24.
(3)铬的化合物可用于检测司机是否酒后驾车,其原理为遇到酒精,红色的CrO3转变为绿色的Cr2(SO4)3,在Cr2(SO4)3中铬元素的化合价为+3.
分析 (1)根据元素与微观粒子及物质的区别进行分析;根据牛奶和鸡蛋清的营养成分进行分析;
(2)根据元素周期表提供的信息分析判断;
(3)根据化合物中各种元素的化合价代数和为零分析判断.
解答 解:(1)“铬中毒”中的铬是指元素;牛奶和鸡蛋清的营养成分主要是蛋白质,这也是牛奶或鸡蛋清解毒的主要原因;
(2)根据表格信息可知该元素的核电荷数为24;
(3)根据在化合物中正负化合价代数和为零,可得Cr2(SO4)3中Cr元素的化合价为:2x+(-2)×3=0,则x=+3;
故答案为:(1)元素;C;(2)24;(3)+3.
点评 此题是有关铬的问题的考查,解题的关键是掌握相关的化学用语以及基础知识,属基础性知识考查题.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
3.人类生活和生产都离不开金属.
(1)指出金属铜的一个性质及其对应的用途.性质导电性,对应的用途用作电线.
(2)要防止铁制品因锈蚀而报废,就要知道铁制品锈蚀的原因.铁制品锈蚀的条件是铁制品与空气(氧气)和水同时接触.
(3)炼铁的固体原料有铁矿石,石灰石和焦炭,炼铁过程中,CO和Fe2O3反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)某课外小组的同学为了探究金属活动顺序,没计如图所示的实验进行研究.

将实验现象填入表中
通过上述实验,你可以得出的结论是金属活动性顺序为Mg>Fe>Cu.此实验中所用稀硫酸的溶质质量分数必须相同,其原因是使反应结论更准确.
(5)为了进一步验证上述结论,甲同学设计以下实验:把铁片投入15%硫酸铜溶液中(如图④),观察到的现象是在铁的表面形成红色物质,同时溶液变为浅绿色.我国古代“湿法冶铜”就是利用这个反应原理,请写出该反应的化学方程式Fe+CuSO4═Cu+FeSO4.
(1)指出金属铜的一个性质及其对应的用途.性质导电性,对应的用途用作电线.
(2)要防止铁制品因锈蚀而报废,就要知道铁制品锈蚀的原因.铁制品锈蚀的条件是铁制品与空气(氧气)和水同时接触.
(3)炼铁的固体原料有铁矿石,石灰石和焦炭,炼铁过程中,CO和Fe2O3反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(4)某课外小组的同学为了探究金属活动顺序,没计如图所示的实验进行研究.

将实验现象填入表中
| 装置编号 | 实验现象 |
| ① | 金属表面无明显现象 |
| ② | 剧烈反应,金属表面产生大量无色气泡,每片逐渐溶解 |
| ③ |
(5)为了进一步验证上述结论,甲同学设计以下实验:把铁片投入15%硫酸铜溶液中(如图④),观察到的现象是在铁的表面形成红色物质,同时溶液变为浅绿色.我国古代“湿法冶铜”就是利用这个反应原理,请写出该反应的化学方程式Fe+CuSO4═Cu+FeSO4.
7.化学影响着社会的发展和我们的生活质量.以下认识中不正确的是( )
| A. | 可用点燃的方法除去二氧化碳气体中混有的少量的一氧化碳 | |
| B. | 生活中常用肥皂水区别硬水和软水 | |
| C. | 粉尘属于空气质量预报的项目 | |
| D. | 可以用塑料水管代替金属水管 |
 图1、图2分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图.请你结合已有的酸、碱知识,判断溴化氢的水溶液显酸性(填“酸性”?“中性”或“碱性”下同),乙醇的水溶液显中性.
图1、图2分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图.请你结合已有的酸、碱知识,判断溴化氢的水溶液显酸性(填“酸性”?“中性”或“碱性”下同),乙醇的水溶液显中性. 实验室用溶质质量分数为10%硫酸钠溶液进行水的电解实验.
实验室用溶质质量分数为10%硫酸钠溶液进行水的电解实验.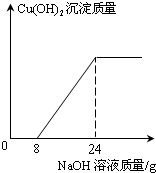 化学兴趣小组的同学监测到一工厂排放的废水中含有H2SO4和CuSO4.为了测定废水中CuSO4的质量分数,该小组取了200g废水,逐滴加入20%的NaOH溶液至过量.测得生成Cu(OH)2沉淀的质量与所加NaOH溶液质量的关系如图所示.
化学兴趣小组的同学监测到一工厂排放的废水中含有H2SO4和CuSO4.为了测定废水中CuSO4的质量分数,该小组取了200g废水,逐滴加入20%的NaOH溶液至过量.测得生成Cu(OH)2沉淀的质量与所加NaOH溶液质量的关系如图所示.