题目内容
14.我市盛产石灰石,主要成分是CaCO3,某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验.取一定量的石灰石样品研碎和100g溶质质量分数为10%的稀盐酸放入烧杯中.在化学反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表:(假设反应匀速进行:杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g.)| 反应时间 | 20 | 40 | 60 | 80 | 100 |
| 烧杯和药品质量/g | 137.8 | 135.6 | m | 134.5 | 134.5 |
(1)表中的“m”为134.5g;
(2)该石灰石中碳酸钙的质量分数.(计算结果精确至0.1%)
分析 (1)根据烧杯和药品质量的变化数据进行分析;
(2)根据质量守恒定律,计算出二氧化碳的质量,然后计算出碳酸钙的质量,再计算质量分数.
解答 解:(1)通过分析表中的数据可以看出,反应时间20-40固体减少了2.2g,所以40-60也可能减少2.2克,但是反应时间80时,固体质量是134.5g,所以m的值是134.5g;
(2)通过分析表中的数据可知,反应前烧杯的总质量为140g,所以石灰石样品质量为140g-100g-25g=15g,
生成二氧化碳为140g-134.5g=5.5g,
设样品中含有碳酸钙为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 5.5g
$\frac{100}{x}$=$\frac{44}{5.5g}$
x=12.5g
所以碳酸钙的质量分数为:$\frac{12.5g}{15g}$×100%=83.3%.
故答案为:(1)134.5;(2)83.3%.
点评 解答本题的关键是能够根据表中提供的数据进行正确的判断,即反应何时进行完全,每次反应生成二氧化碳的质量是多少,这是解题的关键.

练习册系列答案
相关题目
4. 如图分别是氟元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法不正确的是( )
如图分别是氟元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法不正确的是( )
 如图分别是氟元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法不正确的是( )
如图分别是氟元素的原子结构示意图及该元素在元素周期表中的相关信息,下列说法不正确的是( )| A. | 氟元素原子的最外层电子数为7 | B. | 氟元素的原子序数为9 | ||
| C. | 氟元素是非金属元素 | D. | 氟的相对原子质量是19.00g |
5. 向甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
向甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
 向甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
向甲物质中逐渐加入乙物质至过量,若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )| 选项 | 甲物质 | 乙物质 | y轴表示的含义 |
| A | 二氧化锰 | 过氧化氢溶液 | 二氧化猛的质量 |
| B | t℃的水 | 硝酸钾 | t℃时硝酸钾的溶解度 |
| C | 氯化银 | 稀硝酸 | 氯化银的质量 |
| D | 饱和石灰水 | 生石灰 | 溶液的质量 |
| A. | A | B. | B | C. | C | D. | D |
9. 食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富.
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富.
(1)海水晒盐的原理是利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来;
(2)晒盐过程中得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图.t2℃时,MgCl2的溶解度为100g;将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至t1℃时,析出的晶体是MgCl2、KCl(填物质化学式);
(3)将纯净的氯化钠固体配制成溶液,20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解.4组实验数据如下表:
若将②中得到的溶液稀释成质量分数为0.9%的生理盐水,需加水的质量是941g.
关于上述实验的叙述不正确的是D(填序号).
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C.20℃时,氯化钠的溶解度为36g
D.20℃时,将④恒温蒸发25g水,过滤得18g固体.
 食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富.
食盐在生产和生活中具有广泛的用途,是一种重要的资源,海水中储量很丰富.(1)海水晒盐的原理是利用阳光和风蒸发水分,使海水中的水分蒸发掉,使氯化钠结晶出来;
(2)晒盐过程中得到粗盐和卤水.卤水的主要成分及其溶解度的变化如图.t2℃时,MgCl2的溶解度为100g;将t2℃时MgCl2、KCl和MgSO4三种物质的饱和溶液分别降温至t1℃时,析出的晶体是MgCl2、KCl(填物质化学式);
(3)将纯净的氯化钠固体配制成溶液,20℃时,向4个盛有50g水的烧杯中,分别加入一定质量的氯化钠并充分溶解.4组实验数据如下表:
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 4.5 | 9 | 18 | 20 |
| 溶液质量/g | 54.5 | 59 | 68 | 68 |
关于上述实验的叙述不正确的是D(填序号).
A.①②所得溶液是该温度下的不饱和溶液
B.③④所得溶液溶质的质量分数相等
C.20℃时,氯化钠的溶解度为36g
D.20℃时,将④恒温蒸发25g水,过滤得18g固体.
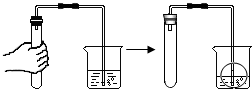 如图所示,龙龙同学采用手握试管外壁的方法检查装置的气密性,若装置的气密性良好,则将双手移开一会后,烧杯内导管处的现象(画圈部分)是( )
如图所示,龙龙同学采用手握试管外壁的方法检查装置的气密性,若装置的气密性良好,则将双手移开一会后,烧杯内导管处的现象(画圈部分)是( )