题目内容
18.“物质的组成与结构决定物质的性质”是科学中的重要观点.按照这一观点讨论下面的问题.(1)酸溶液具有一些共同的化学性质,是因为酸溶液中都含有氢离子;
(2)厨房里的食醋中含有乙酸,它也是一种酸,其主要化学性质是由分子中含有一种叫做“羧基”(如图①中虚线框标出的部分)的结构决定的.据此推测下列②~④的物质中,可能与乙酸具有相似化学性质的是③.(填序号)
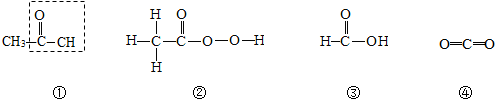
分析 (1)酸的溶液具有共性是因为酸在溶液中都能电离出氢离子.
(2)根据题干提供的信息,物质要具有酸性,需具有“羧基”的结构,然后观察所给物质的结构式即可得出答案.
解答 解:(1)酸的共性是因为酸会在溶液中都电离出相同的阳离子氢离子.
(2)解:食醋中的醋酸具有酸性,其原因是醋酸分子中含有一种叫“羧基”的结构,某物质要具有酸性,需具有“羧基”的结构,分析所给物质的结构式,可知③具有“羧基”的结构,故选③.
故答案为:(1)氢离子 (2)③
点评 题为信息给予题,完成此类题目,要认真阅读题干,抽取有用的信息,结合已有的知识进行.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目
8.工业上侯氏制碱法得到的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验.实验中取30g纯碱样品,平均分成五份(每等分6克)依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,得到的实验数据如下表:(假定反应产生气体全部逸出,其它气体的挥发忽略不计)
(1)第二次加入纯碱样品充分反应后,连同第一次实验共生成二氧化碳4.4克;第三次加入纯碱样品时,是否还能发生化学反应?能.
(2)列式计算纯碱样品中碳酸钠的质量分数.(计算结果精确到0.1%)
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 6 | 6 | 6 | 6 | 6 |
| 电子天平的示数/g | 163.8 | 167.6 | 171.4 | 177.4 | 183.4 |
(2)列式计算纯碱样品中碳酸钠的质量分数.(计算结果精确到0.1%)
6.为了测定某铜锌合金的组成,某校化学课外活动小组利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
(1)试计算该铜锌合金中锌的质量分数.
(2)从上表数据分析,当所取合金与所用稀硫酸的质量比为1:5时,表明合金中的锌与稀硫酸恰好完全反应.
(3)所用合金与稀硫酸恰好完全反应时所得溶液中溶质的质量分数.
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所用稀硫酸的质量/g | 60 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
(2)从上表数据分析,当所取合金与所用稀硫酸的质量比为1:5时,表明合金中的锌与稀硫酸恰好完全反应.
(3)所用合金与稀硫酸恰好完全反应时所得溶液中溶质的质量分数.
13.硝酸钾溶液中混有少量的氢氧化钾,要除去氢氧化钾得到纯净的硝酸钾溶液,下列措施不正确的是( )
| A. | 加入适量硝酸铁溶液 | B. | 加入适量硝酸铜溶液 | ||
| C. | 加入适量硝酸溶液 | D. | 加入适量硫酸溶液 |
3.X、Y两元素的相对原子质量之比为7:2,X与Y形成的化合物中,X、Y两元素的质量之比为21:8,则该化合物的化学式可表示为( )
| A. | X3Y2 | B. | X3Y4 | C. | X2Y3 | D. | XY |
10.下列实验操作中,其中一项的操作目的与其他三项不属于同一类,该项操作是( )
| A. | 闭合电路开关前.将滑片移协到滑动变阻器的阻值最大处 | |
| B. | 做中和反应实验时,事先在碱溶液中滴入1~2滴酚酞试液 | |
| C. | 做氢气还原氧化铜实验时,先通一会儿氢气,把试管中的空气排尽 | |
| D. | 稀释浓硫酸时,要将浓硫酸沿容器壁缓慢注入水中,并用玻璃棒不断搅拌 |
8.下列相对分子质量计算正确的是( )
| A. | NO2:相对分子质量=14×16×2=448 | |
| B. | 2NH3:相对分子质量=2×14+1×3=31 | |
| C. | O2:相对分子质量=16×2=32克 | |
| D. | 2Ca(OH)2:相对分子质量=2[40+(16+1)×2]=148 |