题目内容
20.古语道“人要实,火要虚”,可燃物要架空一些,才能燃烧更旺.火要虚的目的是( )| A. | 增大可燃物热值 | B. | 增大可燃物与空气接触面积 | ||
| C. | 降低可燃物的着火点 | D. | 增大空气中氧气的含量 |
分析 燃烧需要满足三个条件:一是要有可燃物,二是可燃物要与氧气接触,三是温度要达到可燃物的着火点;以上三个条件都能满足时,可燃物才能发生燃烧,可燃物与氧气接触越充分燃烧越完全越剧烈.
解答 解:A、可燃物的热值一般不会改变,故错误;
B、可燃物架空一些,可使空气容易进入而增大可燃物与空气的接触面,使燃烧更完全,燃烧更旺,故正确;
C、可燃物的着火点一般不会发生变化,故错误;
D、空气中氧气的含量一般不会改变,故错误.
故选B.
点评 可燃物燃烧通常需要氧气的支持,可燃物与氧气充分接触或氧气充足时可发生完全燃烧,与氧气接触不充分或氧气不足时则发生不完全燃烧【点评】.

练习册系列答案
相关题目
20.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开始探究活动.以下是教学片断,请你参与学习并帮助填写空格(包括表中空格).
【查阅资料】Na2SO4溶液呈中性
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的,你认为不合理的猜想是哪种并说出理由猜想四H2SO4和NaOH在溶液中不能共存.
【继续试验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴酚酞溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,丙选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一直确定猜想二是正确的.
【评价反思、老师对同学能用多种方法进行探究,并且得出正确结论给予肯定,同时也指出上述三个实验探究中也有一个是不合理的,这个方案是③(选填①、②、③),你还可以选择锌粒(填药品名称)进行实验,也能得出同样的结论.
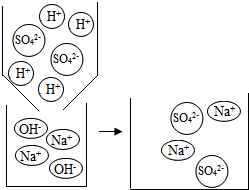
【剖析本质】实验后,老师又带领大家从微观的角度来理解此反应的实质,请你和同学们一起在反应后的方框中补画未画全的微粒.
Ⅰ.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如下实验:
试计算上述【演示实验】反应后溶液中Na2SO4的质量分数是多少?(列出计算过程)
【查阅资料】Na2SO4溶液呈中性
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的,你认为不合理的猜想是哪种并说出理由猜想四H2SO4和NaOH在溶液中不能共存.
【继续试验】(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴酚酞溶液,无明显变化,溶液中一定没有NaOH或氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,丙选用老师提供的pH试纸、铜片、BaCl2溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | ①测溶液pH | ②滴加Na2CO3溶液 | ③滴加BaCl2溶液 |
| 实验现象 | 试纸变色,与标准比色卡比照,得pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思、老师对同学能用多种方法进行探究,并且得出正确结论给予肯定,同时也指出上述三个实验探究中也有一个是不合理的,这个方案是③(选填①、②、③),你还可以选择锌粒(填药品名称)进行实验,也能得出同样的结论.
【剖析本质】实验后,老师又带领大家从微观的角度来理解此反应的实质,请你和同学们一起在反应后的方框中补画未画全的微粒.

Ⅰ.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如下实验:

试计算上述【演示实验】反应后溶液中Na2SO4的质量分数是多少?(列出计算过程)
15.某学生在实验室里,用锌、氧化铜、烯硫酸作原料制取铜,有下列两种途径:
(1)Zn$\stackrel{稀H_{2}SO_{4}}{→}$H2$\stackrel{CuO}{→}$Cu
(2)CuO$\stackrel{稀H_{2}SO_{4}}{→}$CuSO4$\stackrel{Zn}{→}$Cu
若用这两种方法制得的铜的质量相等时,假设反应过程中Zn和稀H2SO4略为过量,下列叙述符合实际实验结果的是( )
(1)Zn$\stackrel{稀H_{2}SO_{4}}{→}$H2$\stackrel{CuO}{→}$Cu
(2)CuO$\stackrel{稀H_{2}SO_{4}}{→}$CuSO4$\stackrel{Zn}{→}$Cu
若用这两种方法制得的铜的质量相等时,假设反应过程中Zn和稀H2SO4略为过量,下列叙述符合实际实验结果的是( )
| A. | 消耗相同质量的氧化铜 | B. | 消耗相同质量的锌 | ||
| C. | 消耗相同质量的硫酸 | D. | 生成硫酸锌的质量可能不同 |
12.下列物质混合后会发生反应,其中不能观察到明显现象的是( )
| A. | 稀盐酸和碳酸钠溶液 | B. | CO2 和氢氧化钠溶液 | ||
| C. | 氢氧化铜和稀硫酸 | D. | 稀硫酸和石蕊溶液 |
10.已知化学反应A+B═C+D,A与B参加反应时质量比为3:2,若反应后生成C和D共50克,则反应用去A的质量为( )
| A. | 49 | B. | 69 | C. | 19 | D. | 30 |