题目内容
9. 在今年沈阳市化学实验操作考查中,我们认真完成了用双氧水和二氧化锰制取氧气的实验,请据此实验回答下列问题.
在今年沈阳市化学实验操作考查中,我们认真完成了用双氧水和二氧化锰制取氧气的实验,请据此实验回答下列问题.(1)要检查A装置的气密性是否良好,通常是把导管口插入水中,然后双手紧握锥形瓶外壁,观察导管口是否有气泡产生.请你回答这种做法依据是什么?(用微粒的观点解释)手握锥形瓶,使瓶内气体受热,微粒运动速率增大,间隔变大,气体体积膨胀,能从导管口逸出.
(2)A装置内发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,二氧化锰在该反应中作催化剂,实验后回收二氧化锰的最佳方法是过滤.
(3)在实验过程中,某同学由于动作太慢,氧气还没有收集满,锥形瓶内的反应就已经停止(如图所示).若想集满这瓶氧气,在不拆卸装置的前提下,请你帮他想出两种方法.
①再加入适量的双氧水使反应继续进行.②从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中.
分析 (1)熟悉微粒的性质之二:运动性、微粒之间有间隔,知道宏观与微观的联系,即:宏观上体积的膨胀与微观上粒子的运动和微粒之间的空隙变大有着密切的关系;
(2)熟记双氧水制取氧气的反应方程式,二氧化锰是催化剂;不溶性固体与液体分离的方法常用过滤;
(3)可再加入反应物,反应就会继续;再者就是将生成物全都收集起来.
解答 解:
(1)根据受热时微粒运动加快,间隔变大的原理,手握锥形瓶,使瓶内气体受热,微粒运动速率增大,间隔变大,气体体积膨胀,能从导管口逸出;
(2)过氧化氢在二氧化锰催化作用下生成水和氧气,反应方程式是:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,二氧化锰是反应的催化剂,能加快过氧化氢的反应速率;因为二氧化锰是固体,双氧水是液体,固体和液体分离要用过滤的方法;
(3)①因为二氧化锰在化学反应前后化学性质不变,所以再加入适量的双氧水反应又会继续;
②因为反应结束后,锥形瓶内仍然有氧气停留,所以可从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中;
故答案为:
(1)手握锥形瓶,使瓶内气体受热,微粒运动速率增大,间隔变大,气体体积膨胀,能从导管口逸出;
(2)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;催化; 过滤;
(3)①再加入适量的双氧水使反应继续进行;
②从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中.
点评 该题主要考查实验室制取氧气的原理、二氧化锰的催化作用、装置气密性检查等知识,掌握相关知识才能结合题意正确解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.以下四种说法正确的是( )
| A. | 燃着的木条伸入盛放某气体集气瓶中熄灭,所以集气瓶中一定是二氧化碳 | |
| B. | 置换反应都有单质生成,所以有单质生成的反应一定是置换反应 | |
| C. | 氧气和臭氧都是氧元素组成的单质,所以不同的物质可能由同种元素组成 | |
| D. | 活泼金属能与稀盐酸反应放出气体,则能与稀盐酸反应放出气体的物质一定是活泼金属 |
17.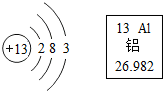 根据右图的信息判断,下列关于铝的说法错误的是( )
根据右图的信息判断,下列关于铝的说法错误的是( )
 根据右图的信息判断,下列关于铝的说法错误的是( )
根据右图的信息判断,下列关于铝的说法错误的是( )| A. | 属于金属元素 | |
| B. | 铝原子的核电荷数是13 | |
| C. | 相对原子质量是26.982 g | |
| D. | 在化学反应中,原子易失去电子形成Al3+ |
4.下列仪器中,不能直接加热的是( )
| A. | 量筒 | B. | 试管 | C. | 蒸发皿 | D. | 烧杯 |
14.用石灰浆抹墙壁后,墙壁变坚硬的原因是( )
| A. | 石灰浆失去水分 | B. | 吸收空气中的水分生成碳酸 | ||
| C. | 生成了生石灰 | D. | 吸收空气中的二氧化碳成碳酸钙 |
1.化学用语是国际通用的化学语言,下列化学用语与含义相符的是( )
| A. | 2H2:4个氢原子 | |
| B. | Fe2+:一个铁离子带2个单位正电荷 | |
| C. | 2O:2个氧元素 | |
| D. | $\stackrel{+2}{CuO}$:氧化铜中铜元素的化合价为+2 |
18.下列各组物质,可由金属与稀盐酸直接反应制取的是( )
| A. | AgCl | B. | FeCl3 | C. | CuCl2 | D. | FeCl2 |
19.下列实验现象描述正确的是( )
| A. | 镁条在氧气中燃烧,生成黑色固体 | |
| B. | 铁丝在空气中燃烧,火星四射,生成黑色固体 | |
| C. | 打开浓盐酸的瓶塞,瓶口产生大量的白烟 | |
| D. | 滴有酚酞的氢氧化钠溶液中加入盐酸,溶液由红色变成无色 |