题目内容
14.利用化学变化可以制备新物质.CO是一种无色、无臭的气体,密度比空气略小,难溶于水,易于血红蛋白结合,具有可燃性.请结合所学知识和CO的相关信息回答下列问题:(1)下列两个反应都能生成CO,从实验室制备气体的思路分析,实验室制备CO选择反应②而不用①的理由是对比反应①、②的条件,反应①的温度更高(任选一个角度回答).
①炽热的焦炭和水蒸气反应:C+H2O$\frac{\underline{\;高温\;}}{\;}$CO↑+H2↑
②草酸晶体和浓硫酸供热:H2C2O4$\frac{\underline{\;浓硫酸\;}}{△}$CO2↑+CO↑+H2O
(2)某同学设计下列装置制备、提纯CO,并用CO来还原氧化铜.请根据如图回答:
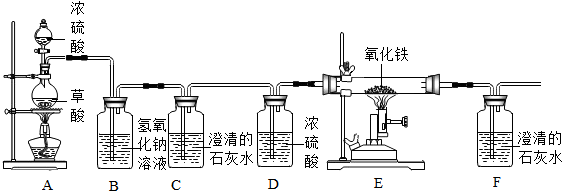
①写出一氧化碳还原氧化铁的化学反应方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②该同学的设计存在的一处明显缺陷是没有尾气处理装置.用改进后装置进行实验,在点燃E处酒精灯之前,必须进行的一项操作是检验一氧化碳的纯度(从实验安全角度考虑).
③装置B的作用是除去CO中混有的CO2,B中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
④证明一氧化碳能还原氧化铁的实验现象是:装置E中固体颜色的变化为红色变为黑色,C中澄清的石灰水没有变浑浊,F中澄清的石灰水变浑浊.
分析 (1)根据反应原理分析解答;
(2)本题是在原有一氧化碳还原氧化铁的实验基础上增加了制取纯净的一氧化碳的实验,由题中信息,草酸分解后得到的一氧化碳中混有二氧化碳和水蒸气,因此要预先除掉二氧化碳.氢氧化钠与二氧化碳反应消耗二氧化碳,浓硫酸具有吸水性除去水分.产生的二氧化碳使澄清石灰水变浑浊,过程中可能一氧化碳过多,必须对尾气进行处理.
解答 解:(1)根据题中信息可知:对比反应①、②的条件,反应①的温度更高;对比反应①、②的混合气体,②比①中的气体更容易分离.
(2)①一氧化碳还原氧化铁的化学反应方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
②一氧化碳有毒,会污染空气,应该有尾气处理装置;一氧化碳点燃时,易发生爆炸,在点燃E处酒精灯之前,必须进行的一项操作是检验一氧化碳的纯度;
③因为要制取纯净干燥的一氧化碳,B装置内是氢氧化钠能吸收产生的二氧化碳,反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O;
④证明一氧化碳能还原氧化铁的实验现象是:装置E中固体颜色的变化为红色粉末变为黑色,B装置内是氢氧化钠能吸收产生的二氧化碳,C是验证二氧化碳是否被吸收完全,澄清的石灰水没有变浑浊,说明没有二氧化碳,生成的二氧化碳通入F中,澄清的石灰水变浑浊.
答案:
(1)对比反应①、②的条件,反应①的温度更高;
(1)①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
②没有尾气处理装置;检验一氧化碳的纯度;
③除去CO中混有的CO2;2NaOH+CO2═Na2CO3+H2O;
④红色粉末变为黑色;澄清的石灰水没有变浑浊;澄清的石灰水变浑浊.
点评 本题考查了炼铁的原理、实验现象、尾气处理以及应用.要注意有毒气体不能随意排放,可燃性气体在加热或点燃前的验纯,以及净化气体的方法.

 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案| A. | 蒸馏水 | B. | 牛奶 | C. | 碘酒 | D. | 番茄酱 |
| A. | 除去氯化钙溶液中的少量盐酸:加入过量的氧化钙 | |
| B. | 区别氯化钠和氯化铵:分别与氢氧化钠溶液混合加热 | |
| C. | 制取氢氧化钾溶液:将氢氧化钙溶液与氯化钾溶液混合后过滤 | |
| D. | 比较稀盐酸和稀醋酸的酸碱度:将pH试纸分别伸入两种液体中观察颜色 |
| A. | M由四种元素组成 | B. | M的化学性质很稳定 | ||
| C. | M中有氨气 | D. | M可能是碳酸氢钠 |
| A. | 4.0g | B. | 3.9g | C. | 3.0g | D. | 2.5g |

| A. | 化学能转变成电能的过程中发生了氧化还原反应 | |
| B. | 若反应中的PbO2和Pb的质量比是239:207,物质X一定是H2SO4 | |
| C. | 充电使电能转化成化学能,充电可降低H2SO4的浓度 | |
| D. | 随意丢弃铅蓄电池会造成土壤和水的污染 |

 如图为铝原子的原子结构示意图及铝元素在元素周期表中的相关信息,请根据图示回答下列有关问题:
如图为铝原子的原子结构示意图及铝元素在元素周期表中的相关信息,请根据图示回答下列有关问题: