题目内容
6.人类生产和生活都离不开金属.早在春秋战国时期,我国就开始生产和使用金属.Ⅰ.随着贵(阳)→广(州)高铁的开通.贵阳已进入高铁时代.高铁建设需要大量的钢铁.那钢铁是怎样炼成的呢?
[原料]赤铁矿(主要成分是氧化铁)、焦炭、空气等.
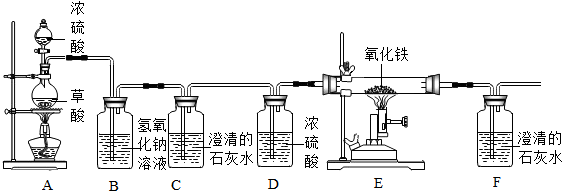
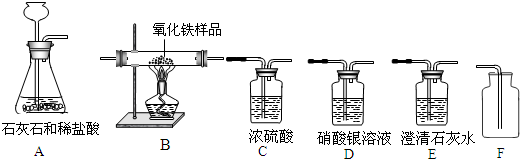
[流程]主要反应过程如图.

[原理](1)反应的化学方程式:①C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,②CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,③Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)反应①中空气要过量,目的是使焦炭完全反应生成二氧化碳.
Ⅱ.锰钢是一种合金,可用于高铁建设.若金属活动性:锰>铁.请设计实验加以验证.
实验方案是将金属锰加入到硫酸亚铁溶液中(不用描述实验现象).
Ⅲ.铝合金不但用于日常生活,还用于火箭、飞机的制造.某铝合金只含铝和另一种金属X.为确定其成分,在实验室将mg该铝合金投入稀硫酸中,发现合金完全溶解,并生成ng氢气,铝与稀硫酸反应的化学方程式为2Al+3H2SO4=Al2(SO4)3+3H2↑.若要确定该合金中金属X的相对原子质量还需要的条件是合金中铝的质量和金属X的化合价.
分析 (1)根据反应的过程来书写化学方程式;
(2)氧气充足,可燃物充分燃烧;
Ⅱ、根据金属的活动性顺序来分析;
Ⅲ、铝和稀硫酸反应生成硫酸铝和氢气,根据合金的组成来分析.
解答 解:(1)①是碳在空气中充分燃烧生成二氧化碳,②是二氧化碳在高温的条件下与碳反应生成一氧化碳,③是氧化铁在高温的条件下反应生成铁和二氧化碳;故填:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO;Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(2)空气过量,氧气充足,碳发生充分燃烧,故填:使焦炭完全反应生成二氧化碳;
Ⅱ、根据活动性强的金属可以把活动性较弱的金属从其盐溶液中置换出来的规律,可以将金属锰加入到硫酸亚铁溶液中,观察现象;故填:将金属锰加入到硫酸亚铁溶液中;
Ⅲ、铝和稀硫酸反应生成硫酸铝和氢气,若要确定该合金中金属X的相对原子质量还需要的条件是合金中铝的质量和金属X的化合价,故填:2Al+3H2SO4=Al2(SO4)3+3H2↑;合金中铝的质量和金属X的化合价.
点评 本题难度不大,掌握铁的冶炼原理、化学方程式的书写方法、金属活动性等是正确解答本题的关键.

练习册系列答案
相关题目
16.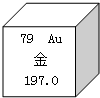 3月18日晚间新闻报道:国家卫计委公开征求意见拟批准金箔用于白酒,最大用量为每公斤0.02克.很多人表示惊讶,“黄金酒”来了.下列对金的说法正确的是( )
3月18日晚间新闻报道:国家卫计委公开征求意见拟批准金箔用于白酒,最大用量为每公斤0.02克.很多人表示惊讶,“黄金酒”来了.下列对金的说法正确的是( )
 3月18日晚间新闻报道:国家卫计委公开征求意见拟批准金箔用于白酒,最大用量为每公斤0.02克.很多人表示惊讶,“黄金酒”来了.下列对金的说法正确的是( )
3月18日晚间新闻报道:国家卫计委公开征求意见拟批准金箔用于白酒,最大用量为每公斤0.02克.很多人表示惊讶,“黄金酒”来了.下列对金的说法正确的是( )| A. | 该元素属于金属元素 | B. | 该原子核外有197个电子 | ||
| C. | 金的相对原子质量为197g | D. | 该元素原子的中子数79 |
17.过多的植物营养物质如尿素CO(NH2)2等进入水体会导致“水华”现象.下列说法不正确的是( )
| A. | 尿素由四种元素组成 | |
| B. | 尿素属于氮肥 | |
| C. | 尿素属于复合肥 | |
| D. | 使用无磷洗衣粉可以减少“水华”现象发生 |
1.下列属于化学变化的是( )
| A. | 酒精挥发 | B. | 纸张燃烧 | C. | 冰雪融化 | D. | 玻璃破碎 |
11.下来有关实验基本操作,正确的是( )
| A. |  点燃酒精灯 | B. | 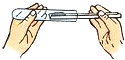 取用固体粉末 | C. | 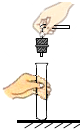 塞紧橡皮塞 | D. |  闻气体气味 |
18.下列环境问题与防治措施说法合理的是( )
| A. | 酸雨-将燃煤锅炉烟囱加高 | B. | 白色污染-废弃塑料袋焚烧处理 | ||
| C. | 雾霾-减少化石燃料的使用 | D. | 水体富营养化-禁止使用化肥 |
15.玉米地的玉米苗叶子发黄,应及时施加的肥料是( )
| A. | KCl | B. | K2SO4 | C. | Ca3(PO4)2 | D. | NH4NO3 |