��Ŀ����
С��ͬѧ���»���ˮ��ͷ����˵�������˽��ˮ��ͷ��ͭ�ʶƸ��������С����̽������Cr���볣����������ͭ�Ļ��ǿ����������һͬ�μӣ�
��֪ʶ�طš�
�������˳��K Ca Na Mg Al Zn����Sn Pb��H������Hg Ag Pt Au�������ں�������д��Ӧ������Ԫ�ط��ţ�
���������롿
����1��Cr��Fe��Cu�� ����2��Fe��Cu��Cr�� ����3����IJ�����������
���������ϡ�
��1����������ɫ�й���Ľ������ڿ���������������ɿ���ʴ�����ܵ�����Ĥ��
��2��������ϡ���ᷴӦ��������ɫ�������Ǹ���CrSO4����Һ��
[���ʵ��]
С��ͬѧȡ��С��ȵ����ֽ���Ƭ����ɰֽ��ĥ��������ȡ��֧�Թܣ��ֱ���������ͬ��ϡ���ᣮ
| ʵ�� | �Թ�1 | �Թ�2 | �Թ�3 |
| ʵ�� ���� |
|
|
|
| ʵ�� ���� | ��Ƭ����������ݽ�������Һ��Ϊdz��ɫ | ��Ƭ����������ݽϿ죬��Һ���Ϊ��ɫ | ���� |
����������͡�
��1��С�ϵõ��Ľ����Dz���������ȷ��
��2��ʵ��ǰ��ɰֽ��ĥ����Ƭ��Ŀ����������
��֪ʶ���á�
����ƬͶ��FeSO4��Һ�У���Ӧ���ܡ�����ܡ����ܡ������У����ܽ��У�����д����Ӧ�Ļ�ѧ����ʽ��4����
| ������Ե�̽������д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��. | |
| ר�⣺ | ѹ��ʵ���⣻������������ϣ� |
| ������ | [֪ʶ�ط�]���ݽ������˳������� [��������]�������ֽ����Ļ��˳����в��룻 [���ʵ��]����ͭ�Ļ��˳��λ����ĺ���������� [���������]��1������ʵ�������ó����ۣ���2�����ݽ����ı��泣��һ������������Ӱ���������Һ�ķ�Ӧ������ [֪ʶ����]�����ڽ������˳���У�λ��ǰ��Ľ����ܰ�λ�ں���Ľ��������ǻ��������Һ���û�����������д����Ӧ�ķ���ʽ�� |
| ��� | �⣺[֪ʶ�ط�]�������˳��Ϊ��K Ca Na Mg Al Zn Fe Sn Pb��H�� Cu Hg Ag Pt Au�� [��������]���ֽ����Ļ��˳����ܴ����������������1ΪCr��Fe��Cu�� ����2ΪFe��Cu��Cr���ʲ���3�𰸣�Fe��Cr��Cu�� [���ʵ��]��Ϊͭ�Ļ��˳��λ����ĺ��棬��˲��ܺ��ᷴӦ������Ϊ������ [���������]��1���Թ�1��ʵ��������Ƭ����������ݽ�������Һ��Ϊdz��ɫ����֪�������ڽ����˳����������ǰ�����ݸ�Ƭ����������ݽϿ죬��Һ��Ϊ��ɫ���Ӷ��ó���Ҳ������ǰ�Ҹ��������ã���Ϊͭ���ܺ�ϡ���ᷴӦ������������֪ͭ������ĺ��棬�ʲ���1��Cr��Fe��Cu��ȷ�� ��2����Ϊ�����ı��泣��һ������������Ӱ���������Һ�ķ�Ӧ�����ʵ��ǰ��ɰֽ��ĥ����Ƭ��Ŀ���dz�ȥ�������������Ĥ�����ڷ�Ӧ�� [֪ʶ����]��Ϊ��������������ǿ���ʸ��ܺ�����������Ӧ�����������������Ӧ�ķ���ʽΪ��Cr+FeSO4=Fe+CrSO4�� �ʴ�Ϊ��[֪ʶ�ط�]Fe�� Cu�� [��������]Fe��Cr��Cu�� [���ʵ��]�������������������������ɣ���ҺҲ����ɫ���� [���������]��1��1����2����ȥ�������������Ĥ�����ڷ�Ӧ�� [֪ʶ����]�ܣ� Cr+FeSO4=Fe+CrSO4�� |
| ������ | �����ǶԽ������˳��Ŀ��飬����ʵ��̽�������Ļ��˳������ʵ��̽���Ĺ��̣�ע��ѧ������ʵ�����ʵ�������������� |

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�С��ͬѧ�Ķ��������ϵ�֪������ͭ���������Ƚ���������Ҳ������Ϊ����������Һ�ֽ���ȡ�����Ĵ�����������ѡ������ͭ������̽��ʵ�飮
��������⡿����ͭ�Ƿ����������������Һ�ֽ���ȡ�����Ĵ����أ����Ƿ�ȶ������̴���Ч�������أ�
�����ʵ�顿С��������40mL������Ϊ�������������ʵ�飺
| ʵ����� | 5%����������Һ���/mL | �������� | ����40mL�������õ�ʱ�� |
| �� | 10 | / | |
| �� | 10 | ����ͭ1.2g | |
| �� | 10 | ��������1.2 |
��1����ʵ���У��������������Ӧѡ���װ��������������ţ���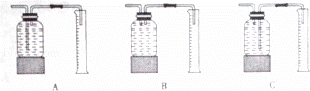
��2����ʵ��ڲ���40mL������ʵ��ٵ�ʱ�����������ࡱ���١�����˵������ͭ�ܼӿ�������ֽ����ʣ�
��3����Ҫ֤������ͭ�ǹ�������ֽ���ȡ�����Ĵ���������Ҫ��֤����ͭ��ʵ����з�Ӧǰ�������δ�����ı䣬С��ͬѧ��ʵ��ڷ�Ӧ��Ĺ�����й��ˡ�ϴ�ӣ��ٳ����õ�1.2g��ɫ��ĩ���ٽ���ɫ��ĩ�����Թ��У�����������������������
��4��������40mL������ʵ��ڵ�ʱ�����ʵ��ۣ�����Եó�������
��Ԥ�ڽ��ۡ�������
����֪ʶ���ɣ���ȫ��ȷ��һ���ǣ�������
| A�������仯 | B�����ӵ���ʶ |
| �ٵ��ˮ�ǽ�����ת���ɻ�ѧ�� ��úȼ���ǽ���ѧ��ת�������� ���ڻ�ѧ��Ӧ��ֻ��ȼ�ղ��ܷų����� | �������穁�����Ӳ����˶� ˮ��ɱ��������Ӽ���ı� ˮ�ĵ�⩁�����ӷ����ı� |
| C�����ֺ��� | D����Դ��Լ |
| ��Fe2+��һ���������Ӵ�2����λ����� ��SO3��һ��������������к���3��ԭ�� �� | �ٷϾɽ����������� ���ᳫʹ���Ҵ����� ��ʵ�����ʣҩƷ�Ż�ԭƿ |
| �� | A�� | �����仯 | B�� | ���ӵ���ʶ | C�� | ���ֺ��� | D�� | ��Դ��Լ |
ˮ��������ԴȪ�������౦�����Դ������ʱ�ܻ��������ƣ���ʱ�ܻ�Ϊ����ϸ�꣮���й����У�����Ϊˮ���ӷ����˱仯���ǣ�������
| �� | A�� | ˮ�������������ˮ | B�� | ���Ǻ�ˮ��Ϻ�õ���ˮ |
| �� | C�� | ˮͨ�������������� | D�� | ��������ˮ |
������ʵ��ָ�������е�ˮ�������û������ˮ����Ҫ���õ��ǣ�������
| A | B | C | D | |
| ʵ��װ�� |
����������ȼ�� |
�ⶨ�������������� |
��˿��������ȼ�� |
��ˮ���ռ����� |
| ���� | ����ƿ�е�ˮ�����շų������� | ��Ͳ�е�ˮ��ͨ��ˮ����ı仯�ó�O2��� | ����ƿ�е�ˮ����ȴ�����������ֹ����ƿը�� | ����ƿ�е�ˮ��ˮ�Ƚ�����ƿ�ڵĿ����ž�������ڹ۲�H2��ʱ�ռ��� |
| �� | A�� | A | B�� | B | C�� | C | D�� | D |



 ��Ϩ��˵��������̼���е�����
��Ϩ��˵��������̼���е����� �� ���ɴ˿���֪�����ԭ���� ����ʹ��о�°�λָ�ȼ�գ�����������
�� ���ɴ˿���֪�����ԭ���� ����ʹ��о�°�λָ�ȼ�գ�����������  ��þԪ����+2��
��þԪ����+2��




 ��100% ��
��100% ��