题目内容
20.下列框图中的物质均为中学化学常见物质,其中A是大理石的主要成分,B是黑色粉末,H是蓝色沉淀.如图是它们之间的转化关系,请回答.
(1)写出下列物质的化学式:BCuOCCO2ECa(OH)2;
(2)写出F+G→H的化学方程式:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)写出B→G的化学方程式:CuO+H2SO4═CuSO4+H2O;
(4)写出物质E的一种用途改良酸性土壤.
分析 根据A是大理石的主要成分,所以A就是碳酸钙,A在高温下又会生成C和D,D能够和水反应产生,E能够和碳酸钠溶液反应,所以D就是氧化钙,氧化钙和水生成氢氧化钙,E就是氢氧化钙,氢氧化钙和碳酸钠生成碳酸钙沉淀和氢氧化钠,所以F就是氢氧化钠,C就是二氧化碳;B是黑色粉末,H是蓝色沉淀,因此B是氧化铜,氧化铜和硫酸反应产生硫酸铜和水,硫酸铜和F反应产生氢氧化铜沉淀,因此F是氢氧化钠溶液,据此完成相关的问题.
解答 解:根据A是大理石的主要成分,所以A就是碳酸钙,A在高温下又会生成C和D,D能够和水反应产生,E能够和碳酸钠溶液反应,所以D就是氧化钙,氧化钙和水生成氢氧化钙,E就是氢氧化钙,氢氧化钙和碳酸钠生成碳酸钙沉淀和氢氧化钠,所以F就是氢氧化钠,C就是二氧化碳;B是黑色粉末,H是蓝色沉淀,因此B是氧化铜,氧化铜和硫酸反应产生硫酸铜和水,硫酸铜和F反应产生氢氧化铜沉淀,因此F是氢氧化钠溶液,带入验证符合转化关系,因此:
(1)根据分析,B是氧化铜,C是二氧化碳,E是氢氧化钙;故填:CuO;CO2;Ca(OH)2;
(2)根据分析,E就是氢氧化钙,故E和Na2CO3溶液反应,即氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.故填:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
(3)根据分析,B是氧化铜,G是硫酸铜,氧化铜能与硫酸反应生成硫酸铜和水,其化学方程式为:CuO+H2SO4═CuSO4+H2O;故填:CuO+H2SO4═CuSO4+H2O;
(4)根据分析,E是氢氧化钙,可以用于改良酸性土壤等;故填:改良酸性土壤.
点评 本题为框图式推断题,解题关键是找准解题的突破口,并从突破口出发,探求知识间的内在联系,应用多种思维方式,进行严密的分析和逻辑推理,推出符合题意的结果.

 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案(1)分类法:利用下列4组物质
A.ZnO、MgO、CO2、Na2O B.Cu、N2、O2、Cl2
C.KNO3、NaHCO3、KClO3、Fe(OH)3 D.H2SO4、H2O、HCl、HNO3
请按要求填写下表空白(填写物质的化学式或分类标准)
| A | B | C | D | |
| 分类标准 | 金属氧化物 | ② | 盐 | ④ |
| 不属于该类别的物质 | ① | Cu | ③ | H2O |
A.通过对CO2+H2O═H2CO3;6CO2+6H2O$\frac{\underline{\;光照\;}}{\;}$ C6H12O6+6O2两个化学反应的对比,你能得出的结论是相同的反应物在不同的反应条件下生成的产物可能不同.
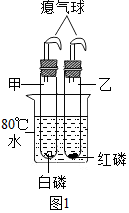
B.如图1所示:小海同学将盛有干燥白磷的甲试管和干燥红磷的乙试管插入盛有80℃的烧杯里(甲、乙试管均套有气球密封).过一会后,发现甲试管中的白磷燃烧,乙试管中的红磷没有燃烧.请根据小海同学的实验现象,对比得出可燃物燃烧所需的条件之一:可燃物温度达到着火点.
(3)归纳演绎法:
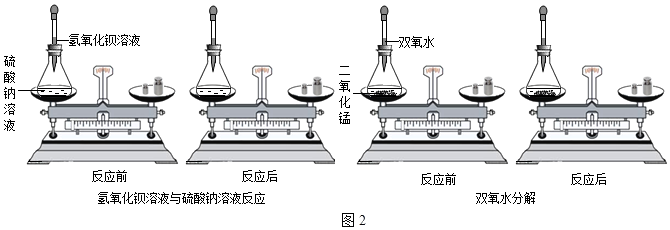
小海同学通过对大量化学反应如氢氧化钡溶液与硫酸钠溶液,双氧水分解(如图2)反应前后各物质的质量总和的测定,得出参加化学反应的各物质的质量总和等于(填“大于”、“小于”或“等于”)反应后生成的各种物质的质量总和.
根据小海得出的结论,可推出7.9g高锰酸钾加热一会后,剩余固体质量为7.5g,则反应生成氧气的质量为0.4g.
| A. | 用一盏燃着的酒精灯点燃另一盏酒精灯 | |
| B. | 闻盐酸的气味时,鼻孔应位于试剂瓶口的正上方 | |
| C. | 氢氧化钠沾到皮肤上,要立即用大量的水冲洗,再涂上3%~5%的硼酸溶液 | |
| D. | 取块状药品时,如果没有镊子可以用手拿 |
[提出问题]:这瓶氢氧化钙是否已经变质?根据已学知识变质原因的化学方程式是CO2+Ca(OH)2=CaCO3↓+H2O.
[猜想]:I.氢氧化钙全部变质;
II.氢氧化钙部分变质;
III.氢氧化钙没有变质.
[设计实验方案、进行实验]:请你选择其中一种猜想参与探究,并填写下表:
| 实验步骤 | 实验现象 | 实验结论 |
| 取样品粉末,加入适量的水,充分搅拌,过滤 ①取少量滤液于试管中,滴入酚酞试液 ②取少量滤渣(或氢氧化钙样品)于试管中,加入盐酸 | ①变红色; ②有气泡生成. | ①氢氧化钙还有剩余; ②说明氢氧化钙与二氧化碳反应有碳酸钙生成. |
[启示与应用]:
①氢氧化钙固体与其溶液都要密封保存.
②根据氢氧化钙水溶液的性质,农业上一般可用氢氧化钙改良酸性土壤(填“酸”或“碱”).
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )| A. | t2℃时,甲、乙两种物质的溶解度相等 | |
| B. | t3℃时,取质量比为1:2的甲、乙的饱和溶液,分别蒸发等质量水后恢复至t3℃,析出溶质的质量甲>乙 | |
| C. | t1℃时,将25g丙加入到50g水中充分溶解能得到不饱和溶液 | |
| D. | 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙 |
| A. | 铁丝在氧气中燃烧时,火星四射、生成黑色固体 | |
| B. | 木炭在氧气中燃烧时,发出红光 | |
| C. | 镁条在空气中燃烧时,发出耀眼的白光 | |
| D. | 硫磺在空气中燃烧时,产生淡蓝色的火焰 |
 如图为甲、乙、丙三种固体物质溶解度曲线,据图回答:
如图为甲、乙、丙三种固体物质溶解度曲线,据图回答: