题目内容
9.我国灿烂的文化历史悠久,源远流长.下列名句中,一定包含有化学变化的是( )| A. | 落霞与孤鹜齐飞,秋水共长天一色 | |
| B. | 春蚕到死丝方尽,蜡炬成灰泪始干 | |
| C. | 只要功夫深,铁杵磨成针 | |
| D. | 不积跬步,无以至千里;不积小流,无以成江海 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:A、落霞与孤鹜齐飞,秋水共长天一色过程中没有新物质生成,属于物理变化.
B、蜡炬成灰泪始干过程中有新物质二氧化碳和水生成,属于化学变化.
C、只要功夫深,铁杵磨成针过程中没有新物质生成,属于物理变化.
D、不积跬步,无以至千里;不积小流,无以成江海过程中没有新物质生成,属于物理变化.
故选:B.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
19.正确的实验操作能保证化学实验的顺利进行.下列实验操作不正确的是( )
| A. | 点燃可燃性的气体之前要先验纯 | |
| B. | 用量筒量取一定量的液体时,视线应与液面最低处相齐 | |
| C. | 加热高锰酸钾制取氧气,用排水法收集完氧气,先将导管移出水面,后停止加热 | |
| D. | 将氢氧化钠固体直接放在托盘天平的托盘上称量 |
20.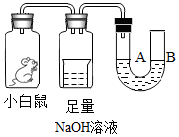 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
 根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )
根据如图来回答:经数小时后,U形管A、B两处的液面会出现下列哪种情况(①假设实验装置足以维持实验过程中小白鼠的生命活动;②瓶口密封且忽略水蒸气和温度变化对实验结果的影响;③NaOH溶液可完全吸收二氧化碳气味)( )| A. | A处上升,B处下降 | B. | A、B两处都下降 | C. | A处下降,B处上升 | D. | A、B两处都不变 |
17.锅炉烧煤时用鼓风机将煤粉吹起,形成沸腾状燃烧.其目的是( )
| A. | 可以降低煤的着火点 | |
| B. | 可以减少有害气体的产生 | |
| C. | 可以使煤成为绿色燃料 | |
| D. | 能增加与氧气的接触面积,能使煤充分燃烧 |
4.研究小组进行木炭还原氧化铁的探究活动.将木炭、氧化铁及试管充分烘干,并将木炭和氧化铁混合均匀、研磨.取适量上述混合物于试管中,用右图1所示的装置加热(试管竖直向上,可使加热时的热量尽少散失).
【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】
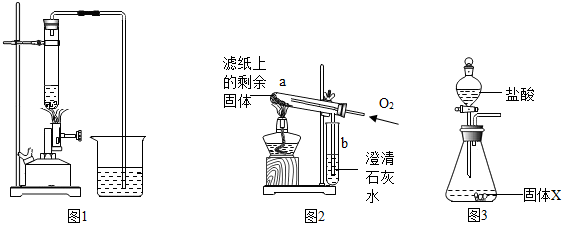
铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁.铁的部分氧化物的性质如下:
Fe3O4具有很好的磁性,能被磁铁吸引.铁的三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl══2FeCl3+3H2O
Fe3O4+8HCl══2FeCl3+FeCl2+4H2O
FeO+2HCl══FeCl2+H2O
黄色的FeCl3溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验FeCl3;FeCl3溶液遇单质铁发生反应:2FeCl3+Fe=3FeCl2,溶液变为浅绿色.
【猜想】固体X可能含有:①Fe ②FeO ③Fe3O4 ④Fe2O3(写化学式) ⑤C
【实施实验】
目的:确定固体X的组成.
【反思改进】
同学们讨论发现,用上述实验方法不能确定固体X中一定没有Fe3O4,理由是固体X中如果含有Fe3O4,步骤V中加盐酸后,由于铁与FeCl3反应生成FeCl2,遇KSCN溶液也不变血红色.
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
【获得结论】
(1)为确定固体X中是否含Fe3O4,m1~m4中应该用到的数据有m1、m2、m3和m4.
(2)固体X各成分的质量比为11:168.
【提出问题】实验结束后,试管中的剩余固体X含有哪些成分,质量分别是多少?
【查阅资料】

铁的氧化物被还原时,是从高价铁的氧化物逐级还原成低价铁的氧化物,最后还原成金属铁.铁的部分氧化物的性质如下:
Fe3O4具有很好的磁性,能被磁铁吸引.铁的三种氧化物均不溶于水,但能溶于稀盐酸,分别发生如下反应:
Fe2O3+6HCl══2FeCl3+3H2O
Fe3O4+8HCl══2FeCl3+FeCl2+4H2O
FeO+2HCl══FeCl2+H2O
黄色的FeCl3溶液中滴入无色的KSCN溶液,溶液变为红色,该实验常用于检验FeCl3;FeCl3溶液遇单质铁发生反应:2FeCl3+Fe=3FeCl2,溶液变为浅绿色.
【猜想】固体X可能含有:①Fe ②FeO ③Fe3O4 ④Fe2O3(写化学式) ⑤C
【实施实验】
目的:确定固体X的组成.
| 步骤 | 操作 | 主要现象 | 结论 |
| I | 取部分冷却后的固体X倒在滤纸上,用磁铁充分吸引. | 部分固体被吸引到磁铁上 | 可能有Fe或Fe3O4 |
| II | 取滤纸上的剩余固体少量,放入图2所示的试管a中,通入氧气,用酒精灯加热. | 固体剧烈燃烧,b中溶液变浑浊 | 一定有C. |
| III | 另取滤纸上的剩余固体少量,放入试管中,加入足量的稀盐酸. | 无明显现象 | 一定没有FeO和Fe2O3 . |
| IV | 取步骤I磁铁上的固体少量,放入试管中,逐滴加入稀盐酸. | 产生产生气泡. | 一定有Fe |
| V | 在步骤IV所得溶液中逐滴加入KSCN溶液. | 溶液不变红色 | 一定没有Fe3O4 |
同学们讨论发现,用上述实验方法不能确定固体X中一定没有Fe3O4,理由是固体X中如果含有Fe3O4,步骤V中加盐酸后,由于铁与FeCl3反应生成FeCl2,遇KSCN溶液也不变血红色.
为确定固体X中是否含Fe3O4并测定其中各成分的质量,同学们又进行了以下实验:
| 步骤 | 操作 | 数据 |
| I | 重新取部分冷却至室温的固体X,称量其质量为m1. | m1=17.9g |
| II | 将称量好的固体X全部放入图3所示的锥形瓶中,称量整套装置及药品的质量为m2;打开分液漏斗旋塞,放入足量稀盐酸后关闭旋塞,待没有气泡产生并恢复至室温,再次称量整套装置及药品的质量为m3. | m2=317.9g m3=317.3g |
| III | 将锥形瓶中剩余的固体过滤、洗涤并干燥,称量其质量为m4. | m4=1.1g |
(1)为确定固体X中是否含Fe3O4,m1~m4中应该用到的数据有m1、m2、m3和m4.
(2)固体X各成分的质量比为11:168.
14.世界是物质的,物质处在不停的运动和变化之中.下列变化中,与其它三种变化有本质区别的是( )
| A. | 铁生锈 | B. | 木柴燃烧 | ||
| C. | 高粱酿酒 | D. | 氧气加压后变成液态氧 |
1.在实验室的下列做法中正确的是( )
| A. | 实验用剩的药品,不要抛弃,不要带出实验室,应放回原试剂瓶 | |
| B. | 加热后的试管立即用冷水冲洗 | |
| C. | 倾倒试液时,为了能看到标签,标签背对着手心 | |
| D. | 给试管里的液体加热时,试管口不能朝着任何人 |
18.一块质量为4克的合金,与足量的盐酸反应完全后生成氢气0.2克,则该合金可能是( )
| A. | 铁镁 | B. | 铁铜 | C. | 铁锌 | D. | 镁铝 |
 下面示意图形象地表示了某化学反应前后分子的变化.其中“○”表示氧原子、“●”表示碳原子,则:该反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.
下面示意图形象地表示了某化学反应前后分子的变化.其中“○”表示氧原子、“●”表示碳原子,则:该反应的化学方程式为:2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2.