题目内容
18.用下列装置进行实验,能达到实验目的是( )| A. |  铁丝在氧气中燃烧 | B. |  检验二氧化碳 | ||
| C. |  测溶液pH值 | D. |  过滤 |
分析 A、根据铁丝在氧气中燃烧的注意事项分析判断;
B、常用澄清的石灰水检验二氧化碳气体;
C、根据测溶液pH值方法分析;
D、根据过滤的要点分析判断.
解答 解:A、瓶底未加上少量的水或细砂,生成的熔化物会炸裂瓶底,故A错误;
B、常用澄清的石灰水检验二氧化碳气体,故B错误;
C、由图示可知,测溶液pH值的方法正确;故C正确;
D、过滤的操作应注意“一贴二低三靠”,图中未用玻璃棒引流、漏斗的下端未紧靠烧杯的内壁,故D错误.
故选C.
点评 本题的难度不大,掌握常见实验的注意事项和操作要点是解答本题的基础.

练习册系列答案
相关题目
6.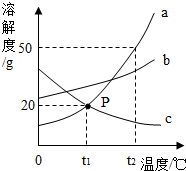 如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )
如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )
 如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )
如图是三种固体物质a、b、c的溶解度曲线,则以下说法不正确的是( )| A. | t1℃时三种物质溶解度的大小为b>a=c | |
| B. | 将t2℃时a的饱和溶液150g降温到t1℃时,析出溶质30g | |
| C. | 除去a物质中的少量c,通常采用蒸发结晶的方法 | |
| D. | t2℃时1g a物质加入到2g水中不断搅拌,能形成3g饱和溶液 |
13.为探究中和反应是否放出热量,甲、乙、丙、丁四位同学选择了不同的药品进行实验,你认为药品选择正确的是( )
| 药品 | |
| 甲 | 浓硫酸和氢氧化钠固体 |
| 乙 | 浓硫酸和氢氧化钠溶液 |
| 丙 | 稀硫酸与氢氧化钠固体 |
| 丁 | 稀硫酸与氢氧化钠溶液 |
| A. | 甲 | B. | 乙 | C. | 丙 | D. | 丁 |
3.某小组同学用盐酸和氢氧化钙,对酸和碱的中和反应进行探究.请你参与.
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由红色变为无色.结论:两种物质发生了反应.反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
【提出问题】甲实验后的溶液中有什么溶质?
【作出猜想】猜想一,只有CaCl2;猜想二有CaCl2和Ca(OH)2;猜想三,有CaCl2和HCl.
【实验探究】为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
【实验结论】丙认为猜想三正确.
【实验评价】丙的实验操作和方案中有不足之处,其不足之处是方案1中使用pH试纸的操作不对;方案2中加AgNO3产生白色沉淀说明溶液中有Cl-,并不能说明溶液中一定有CaCl2.
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为先有气体产生,后有白色沉淀生成.实验中观察到的现象涉及的反应化学方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl(任意写一个).
甲同学向装有氢氧化钙溶液的烧杯中加入盐酸,无明显现象.结论:两种物质未发生反应.乙同学向滴有酚酞的氢氧化钙溶液的试管中慢慢滴加盐酸,溶液由红色变为无色.结论:两种物质发生了反应.反应的化学方程式为Ca(OH)2+2HCl=CaCl2+2H2O.
大家认为乙的实验证明盐酸与氢氧化钙发生了中和反应.并对甲的实验继续探究.
【提出问题】甲实验后的溶液中有什么溶质?
【作出猜想】猜想一,只有CaCl2;猜想二有CaCl2和Ca(OH)2;猜想三,有CaCl2和HCl.
【实验探究】为验证猜想,丙同学设计了方案1和方案2,并按方案进行实验.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作(分别取少量甲实验后的溶液于试管中) | 镊子pH试纸 | AgNO3溶液 | Na2CO3溶液 |
| 实验现象 | 对比标准比色卡:pH<7 | 产生白色沉淀 | |
| 实验结论 | 溶液中有HCl | 溶液中有CaCl2 |
【实验评价】丙的实验操作和方案中有不足之处,其不足之处是方案1中使用pH试纸的操作不对;方案2中加AgNO3产生白色沉淀说明溶液中有Cl-,并不能说明溶液中一定有CaCl2.
大家讨论后通过方案3即证明了猜想三正确,其实验中应观察到的现象为先有气体产生,后有白色沉淀生成.实验中观察到的现象涉及的反应化学方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl(任意写一个).
10.下列实验操作中,能达到实验目的是( )
| A. |  过滤 | B. |  加热液体 | ||
| C. |  除去CO中的水蒸气 | D. |  量取9.3mL液体 |
7.下列图象正确的是( )
| A. |  稀释浓硫酸 | |
| B. |  O2的溶解度曲线 | |
| C. |  等质量的Mg和Fe与足量同浓度稀盐酸反应 | |
| D. |  浓盐酸露置在空气中 |
8.将Cu、CuO、Cu(OH)2 的混合物12g加入到稀硫酸中,恰好完全反应后,过滤,得到含硫元素的6%的溶液50g和滤渣4g,则原混合物中Cu元素的质量分数为( )
| A. | 33% | B. | 30% | C. | 83.3% | D. | 70% |