题目内容
5.有一包白色固体粉末,可能含有CuSO4、BaCl2、Na2SO4、Na2CO3、NaCl中的一种或几种,某同学对其组成进行了探究,过程如图,则( )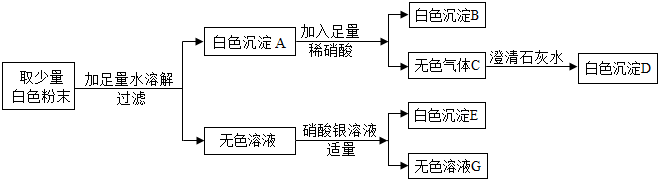
| A. | 无色溶液F中只有NaCl | |
| B. | 沉淀B的化学式为BaSO4 | |
| C. | 原混合物中一定不含CuSO4 | |
| D. | 原混合物中一定含有BaCl2、Na2SO4、Na2CO3 |
分析 根据硫酸铜在溶液中显蓝色,碳酸钠和氯化钡会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀,二氧化碳能使澄清石灰水变浑浊氯离子和银离子会生成氯化银沉淀等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,碳酸钠和氯化钡会生成溶于酸的碳酸钡沉淀,硫酸钠和氯化钡会生成不溶于酸的硫酸钡沉淀,二氧化碳能使澄清石灰水变浑浊氯离子和银离子会生成氯化银沉淀.
取白色粉末加水溶解,得到无色溶液F和白色沉淀A,沉淀A加硝酸会生成是澄清石灰水变浑浊的气体,部分沉淀不溶解,所以白色沉淀A是硫酸钡沉淀和碳酸钡沉淀的混合物,白色粉末中一定含有氯化钡、碳酸钠、硫酸钠,硫酸铜在溶液中显蓝色,所以白色粉末中一定不含硫酸铜,加入硝酸银会生成不溶于酸的白色沉淀,所以F中含有氯化钠,但是氯化钠和硫酸钠、碳酸钠都会生成氯化钠,题中的现象不能确定后粉末中是否含有氯化钠,所以
A、题中的现象不能确定各种物质是否完全反应,所以无色溶液F中一定有NaCl,可能含有氯化钡,或硫酸钠,或碳酸钠,故A错误;
B、通过推导可知,沉淀B不溶于酸,所以沉淀B的化学式为BaSO4,故B正确;
C、通过推导可知,原混合物中一定不含CuSO4,故C正确;
D、通过推导可知,原混合物中一定含有BaCl2、Na2SO4、Na2CO3,故D正确.
故选:A.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
16.下列操作中,能鉴别空气、氧气和二氧化碳三瓶气体的是( )
| A. | 插入燃着的木条 | B. | 观察气体颜色 | C. | 闻气体的气味 | D. | 倒入澄清石灰水 |
13.汽泡爽原料中的柠檬酸(C6H8O7)和小苏打(NaHCO3)粉末混合后加水,可以发生以下反应,推测短线上应填写的化学式为:3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3X.( )
| A. | Al2O3 | B. | NaCl | C. | SO2 | D. | CO2 |
10.环保部门为了使城市生活垃圾得到合理利用,近年来实施了生活垃圾分类投放的办法.其中塑料袋、废纸、旧橡胶制品等属于( )
| A. | 无机物 | B. | 有机物 | C. | 盐类 | D. | 非金属单质 |
17.用生铁制造的地下管道,在不同环境里被腐蚀的速度最慢的是( )
| A. | 干燥板结的土壤 | B. | 含碳粒较多的潮湿土壤 | ||
| C. | 潮湿的酸性土壤 | D. | 疏松透气的潮湿土壤 |
14.正确使用托盘天平是进行各种化学定量实验的基础,下列操作不正确的是( )
| A. | 称取药品时,药品不能直接放在托盘上 | |
| B. | 称取药品时,药品放在右盘,砝码放在左盘 | |
| C. | 指针停在分度盘中央或左右摆动幅度相等时,天平己平衡 | |
| D. | 使用结束后,应在天平托盘的托架下垫上橡胶垫 |
15.下表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | CaO | CaCO3 | 加水溶解,过滤 |
| B | FeCl2溶液 | CuCl2 | 加入足量铁粉,充分反应后过滤 |
| C | NaCl | KNO3 | 加热水溶解,降温结晶,过滤 |
| D | Cu | Zn | 加入足量稀盐酸,充分反应后过滤,洗涤要,烘干 |
| A. | A | B. | B | C. | C | D. | D |
 下列物质均为初中常见物质,其中B能使带火星小木条复燃,B为黑色固体单质,C为黑色固体氧化物,F为紫红色固体单质,E为铁锈的主要成份,G能使澄清石灰水变浑浊,试回答下列问题:
下列物质均为初中常见物质,其中B能使带火星小木条复燃,B为黑色固体单质,C为黑色固体氧化物,F为紫红色固体单质,E为铁锈的主要成份,G能使澄清石灰水变浑浊,试回答下列问题: