题目内容
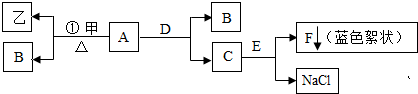
14.粗盐中含泥沙、氯化钙、氯化镁等杂质,某同学用自制的简易净水器提纯粗盐,效果不理想.用自制的简易净水器净化后的粗盐水仍含可溶性杂质,他设计了如图的除杂流程:
(1)步骤①反应的化学方程式为MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;
(2)步骤②反应的化学方程式为CaCl2+Na2CO3═CaCO3↓+2NaCl、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)步骤③操作a的名称是过滤,步骤④加入适量盐酸的目的是除去滤液中的Na2CO3和氢氧化钠.
(4)最后从精盐水中提取食盐可采取蒸发操作.
分析 (1)步骤①,即氢氧化钙与氯化镁溶液反应生成氢氧化镁沉淀和氯化钙,进行分析解答.
(2)步骤②,即碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
(3)步骤③中操作a是将沉淀与滤液分离,步骤④加入适量盐酸,能与过量的碳酸钠和氢氧化钠反应,进行分析解答.
(4)根据氯化钠的溶解度受温度影响变化不大,进行分析解答.
解答 解:(1)步骤①,即氢氧化钙与氯化镁溶液反应生成氢氧化镁沉淀和氯化钙,反应的化学方程式为:MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2.
(2)步骤②,即碳酸钠与氯化钙反应生成碳酸钙沉淀和氯化钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式分别为:CaCl2+Na2CO3═CaCO3↓+2NaCl、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)步骤③中操作a是将沉淀与滤液分离,操作a的名称是过滤;步骤④加入适量盐酸,能与过量的碳酸钠和氢氧化钠反应,目的是除去滤液中的Na2CO3和氢氧化钠.
(4)氯化钠的溶解度受温度影响变化不大,最后从精盐水中提取食盐可采取蒸发结晶的方法.
故答案为:(1)MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2;
(2)CaCl2+Na2CO3═CaCO3↓+2NaCl、Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
(3)过滤;氢氧化钠;
(4)蒸发.
点评 本题难度不大,掌握粗盐提纯的原理、盐的化学性质、化学方程式的书写方法等并能灵活运用是正确解答本题的关键.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案
相关题目
15.空气是构成地球周围大气的气体,无色、无味,下列关于空气的说法中正确的是( )
| A. | 空气属于混合物 | B. | 空气中氧气的含量约占30% | ||
| C. | 空气没有自动净化能力 | D. | 空气中的氧气化学性质活泼 |
19.空气中氧气含量测定的再认识.

【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的文字表达式磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内压强减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe (OH)2],写出该反应的化学方程式2Fe+O2+2H2O=2Fe(OH)2.
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者(用红磷燃烧来测定空气中氧气含量)准确度更髙的原因是:①氧气完全反应;②避免了燃烧匙伸入集气瓶中时导致的空气外逸.

【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的文字表达式磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内压强减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe (OH)2],写出该反应的化学方程式2Fe+O2+2H2O=2Fe(OH)2.
(2)根据表中数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者(用红磷燃烧来测定空气中氧气含量)准确度更髙的原因是:①氧气完全反应;②避免了燃烧匙伸入集气瓶中时导致的空气外逸.
3.小明最近身体不适,医生建议多补充维生素.他应该适量增加的食物是( )
| A. | 水果和蔬菜 | B. | 鸡蛋和肉 | C. | 花生油和奶油 | D. | 馒头和稀饭 |