题目内容
4.将30g碳酸钠溶液与48.2g氯化钡溶液混合,碳酸钠和氯化钡两种物质恰好完全反应.过滤,所得滤液质量为58.5g,试计算:所得滤液中溶质的质量分数为多少?(反应的化学方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl)
分析 碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,反应前后的质量差即为生成沉淀碳酸钡的质量,根据碳酸钡的质量可以计算氯化钠的质量,进一步可以计算所得滤液中溶质的质量分数.
解答 解:设所得滤液中NaCl的质量为x,
根据质量守恒定律,生成BaCO3的质量为30g+48.2g-58.5g=19.7g,
Na2CO3+BaCl2=BaCO3↓+2NaCl,
197 117
19.7g x
$\frac{197}{19.7g}$=$\frac{117}{x}$,
x=11.7g,
滤液中溶质的质量分数为:$\frac{11.7g}{58.5g}$×100%=20%,
答:所得滤液中溶质的质量分数为20%.
点评 反应前溶液的质量和和反应后滤液的质量差就是反应生成沉淀碳酸钡的质量,这是计算的基础,要注意理解.

练习册系列答案
相关题目
15.2013年“6•5”世界环境日中国主题为“同呼吸 共奋斗”. 倡导在一片蓝天下生活、呼吸的每一个人都应树立保护生态环境的理念,履行好呵护环境的责任.下列行为不符合这一主题的是( )
| A. | 提倡公交出行,少开私家车 | B. | 实施绿化工程,防治扬尘污染 | ||
| C. | 家用电器不用时,保持待机状态 | D. | 家庭照明使用节能灯,节约能源 |
19. 为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示:下列说法正确的是( )
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示:下列说法正确的是( )
 为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示:下列说法正确的是( )
为减少污染、提高煤的利用率,可将其转化为可燃性气体,其微观示意图如图所示:下列说法正确的是( )| A. | 图中表示化合物的是“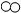 ” ” | |
| B. | 反应物与生成物均由分子构成 | |
| C. | 该反应中反应物两种分子的个数比为3:1 | |
| D. | 反应前后原子的种类和数目保持不变 |
9.月球是人类未来研究宇宙的理想基地.假如你有幸成为一名登上月球的宇航员,你认为在月球上,下列猜想不正确的是( )
| A. | 抛出去的重物依旧会降落到月球表面 | |
| B. | 晚上,可以在月球上生堆篝火取暖 | |
| C. | 月球上你很容易把50kg的重物高举过头顶 | |
| D. | 如果月球上的物质中含有氧元素,就有希望在月球上制取氧气 |
16.以下几种实验操作,不正确的是( )
| A. |  酒精灯失火用湿抹布扑盖 | B. |  测定未知溶液的pH | ||
| C. |  加碱研磨后闻气味鉴别铵态氮肥 | D. |  分离溶液中析出的KNO3晶体 |
14.下列物质放入水中,能形成溶液的是( )
| A. | 面粉 | B. | 牛奶 | C. | 白糖 | D. | 花生油 |
