题目内容
8.石灰石的主要成分是CaCO3(其余杂质不溶于水,亦不参加反应).某化学兴趣小组为了测定石灰石中CaCO3的质量分数,进行了以下探究实验:称石灰石样品二份,分别放入大烧杯中,第一个烧杯中加入50克稀盐酸,第二个烧杯中放入100克稀盐酸,充分反应至不再有气泡产生时称量残留物质量,有关数据如表.求:(1)二个烧杯中产生CO2的质量(填入表中);
(2)石灰石样品中CaCO3的质量分数.
(3)稀盐酸中溶质的质量分数.
| 各物质的质量 | 第一个烧杯 | 第二个烧杯 |
| 石灰石样品质量 | 12g | 12g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 58.7g | 107.6g |
| 产生的CO2质量 | 3.3g | 4.4g |
分析 (1)根据质量守恒定律可以计算出二氧化碳的质量;
(2)根据在化学方程式中二氧化碳的质量,可以计算碳酸钙的质量;
(3)利用碳酸钙的质量对恰好反应时消耗的氯化氢质量进行计算,则可得盐酸的溶质质量分数;
解答 解:(1)第一个烧杯中产生二氧化碳的质量为:12g+50g-58.7g=3.3g,
第二个烧杯中产生二氧化碳的质量为:12g+100g-107.6g=4.4g,
填表如下:
| 各物质的质量 | 第一个烧杯 | 第二个烧杯 |
| 石灰石样品质量 | 12g | 12g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 58.7g | 107.6g |
| 产生的CO2质量 | 3.3g | 4.4g |
由表中数据可知,第二个烧杯中的碳酸钙完全反应,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x=10g,
石灰石样品中CaCO3的质量分数为:$\frac{10g}{12g}$×100%=83.3%,
(3)由表中数据可知,第一个烧杯中的盐酸完全反应,
设稀盐酸中HCl 的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑
73 44
y 3.3g
$\frac{73}{y}=\frac{44}{3.3g}$
y≈5.5g
稀盐酸中HCl的质量分数=$\frac{5.5g}{50g}×$100%=11%.
答案:
(1)
| 各物质的质量 | 第一个烧杯 | 第二个烧杯 |
| 石灰石样品质量 | 12g | 12g |
| 稀盐酸质量 | 50g | 100g |
| 烧杯残留物质量 | 58.7g | 107.6g |
| 产生的CO2质量 | 3.3g | 4.4g |
(3)稀盐酸中溶质的质量分数为11%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析表中数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.如图所示各组转化中,一定条件下均能一步实现的组合是( )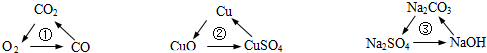

| A. | ①② | B. | ①③ | C. | ②③ | D. | ①②③ |
3.对比归纳是学习化学的重要方法.请你参与下列探究活动并回答问题:
| 实验一:探究影响硫燃烧剧烈程度的因素. | 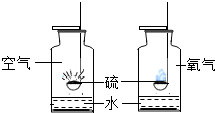 | (1)硫在氧气中燃烧的化学方程式为S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2; (2)硫在氧气中燃烧比在空气里更剧烈,说明影响硫燃烧剧烈程度的因素是氧气的浓度. |
| 实验二:验证Fe>Cu>Ag金属活动性顺序 | 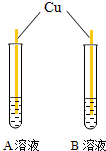 | (3)试管中A、B溶液的溶质为Fe(NO3)2、AgNO3(填化学式); 有关反应的化学方程式Cu+2AgNO3→Cu(NO3)2+2Ag. |
| 实验三:探究影响物质溶解性的因素. | 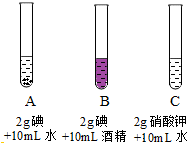 | (4)振荡静置:B中固体易溶,A中几乎不溶.物质的溶解性与溶剂的种类 有关; (5)A与C比较,控制的变量有温度、等体积的水等. |
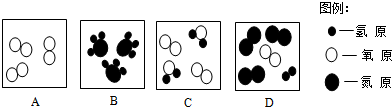
13.知识推理是我们在化学学习中学到的重要的方法,但不符合事实的推理会得出错误的结论.下列推理正确的是( )
| A. | CO2、H2O都是由分子构成,所以NaCl也是由分子构成的 | |
| B. | 氢气与空气混合点燃可能发生爆炸,所以CH4与空气混合点燃也可能发生爆炸 | |
| C. | 硝酸铵溶于水会吸收大量的热,使溶液温度降低,所以食盐溶于水也吸收大量的热 | |
| D. | 氮肥NH4Cl与熟石灰研磨放出氨气,所以含氮肥料KNO3与熟石灰研磨也能放出氨气 |
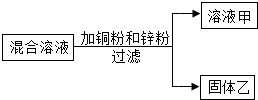 某化学小组向一定量AgNO3和Al(NO3)3的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2;②固体乙中一定含有Ag,可能含有Cu和Zn;③若溶液甲是蓝色,则溶液甲一定含Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④向固体乙滴加稀盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2,上述四种说法正确的个数为( )
某化学小组向一定量AgNO3和Al(NO3)3的混合溶液中加入铜粉和锌粉,充分反应后过滤,得到溶液甲和固体乙,如图所示,则:①溶液甲中一定含有Al(NO3)3和Zn(NO3)2;②固体乙中一定含有Ag,可能含有Cu和Zn;③若溶液甲是蓝色,则溶液甲一定含Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④向固体乙滴加稀盐酸有气泡产生,则溶液甲中一定没有AgNO3和Cu(NO3)2,上述四种说法正确的个数为( )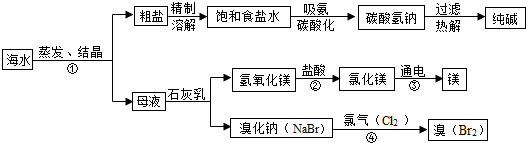
 现有一瓶久置的过氧化氢溶液(标签如图所示),已知过氧化氢溶液在存放过程中会缓慢分解,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g.
现有一瓶久置的过氧化氢溶液(标签如图所示),已知过氧化氢溶液在存放过程中会缓慢分解,取该溶液34g于烧杯中,加入一定量的二氧化锰,完全反应后,称得烧杯内剩余物质的总质量是33.8g,将杯内剩余物质过滤、洗涤、干燥后得滤渣3g.