题目内容
6.合理化处理废水是当前防治废水中的有害或有毒物质对环境造成污染的重要举措.某化学试剂厂甲、乙、丙、丁四个车间排放的废水中,主要成分分别含有CuCl2、HCl、Na2CO3、NaOH的一种.甲车间的废水呈蓝色.通过调节废水流量,使乙、丁两个车间废水相对过量,最终排出的废水呈中性.处理过程如图所示,在第①反应池中出现大量的蓝色沉淀,在第②反应池中出现大量的气泡.请回答:
(1)甲车间排放的废水主要成分是CuCl2.
(2)第③反应池排放的中性废水中的溶质是NaCl(用化学式表示).
分析 根据甲车间的废水呈蓝色,可以确定车间排放的废水主要成分是CuCl2;由于丙、丁车间的废水反应池中出现大量的气泡,丁车间的废水过量,反应后废水呈酸性,所以丙的废水主要成分是碳酸钠,丁的废水主要成分是盐酸,乙的废水主要成分是氢氧化钠,据此分析回答有关的问题.
解答 解:由题意可知,甲车间的废水呈蓝色,可以确定车间排放的废水主要成分是CuCl2;由于丙、丁车间的废水反应池中出现大量的气泡,丁车间的废水过量,反应后废水呈酸性,所以丙的废水主要成分是碳酸钠,丁的废水主要成分是盐酸,乙的废水主要成分是氢氧化钠.由于氯化铜与氢氧化钠反应生成了氢氧化铜沉淀和氯化钠,碳酸钠与盐酸反应生成了氯化钠二氧化碳和水,过量的氢氧化钠与盐酸反应生成了氯化钠.所以第③反应池排放的中性废水中的溶质是氯化钠.由此可知:
(1)甲车间排放的废水主要成分是 CuCl2.
(2)第③反应池排放的中性废水中的溶质是NaCl.
故答为:(1)CuCl2;(2)NaCl.
点评 在解此类题时,先根据两两反应的酸碱性推测废水的组成,然后再结合题中的条件进行验证即可.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14. 如图是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( )
如图是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( )
 如图是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( )
如图是探究铁锈蚀条件的装置.调节L端与R端的液面高度一致,塞紧木塞,一周后观察.下列推断错误的是( )| A. | b管中铁钉不容易锈蚀 | |
| B. | 铁锈蚀可能与空气、水有关 | |
| C. | L端与R端液面高度仍然保持一致 | |
| D. | a管中浸没在水中的那部分铁钉不容易锈蚀 |
1.下列实验基本操作正确的是( )
| A. | 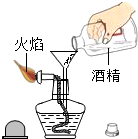 | B. | 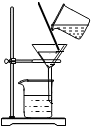 | C. | 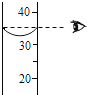 | D. | 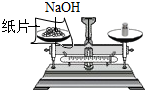 |
11.有A、B两种混合粉末,质量分别为m1,m2.A由CaCO3和KHCO3组成,B由MgCO3和NaHCO3组成.将A、B分别与足量稀盐酸反应,生成二氧化碳气体的质量均为wg.下列说法正确的是( )
(已知:KHCO3+HCl═KCl+CO2↑+H2O NaHCO3+HCl═NaCl+CO2↑+H2O)
(已知:KHCO3+HCl═KCl+CO2↑+H2O NaHCO3+HCl═NaCl+CO2↑+H2O)
| A. | m1=m2 | |
| B. | 25m1=21m2 | |
| C. | 混合物A中CaCO3和KHCO3质量比一定为1:1 | |
| D. | 混合物B中MgCO3和NaHCO3质量比可为任意比 |
15.物质是由肉眼看不到的分子、原子和离子等微观粒子构成的.如图是甲烷气体发生反应的微观示意图,下列说法错误的是( )
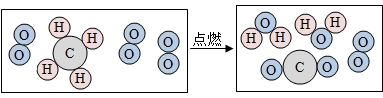

| A. | 该反应中甲烷分子和水分子的个数比是1:2 | |
| B. | 该反应的生成物有3种物质 | |
| C. | 该反应发生的条件是点燃,化学反应前后原子的种类和数目不变 | |
| D. | 该模型可说明:化学变化的实质是分子分成原子,原子重新组合成新分子 |
12.加热条件下,将24g CuO、Fe2O3的混合物与充足的CO完全反应,并将反应后的气体全部通入到澄清石灰水中,得到白色沉淀40g.下列有关叙述中不正确的是( )
| A. | 原混合物中CuO与Fe2O3物质的量的比为1:1 | |
| B. | 反应后所得CO2的质量为40g | |
| C. | 参加反应的CO的质量为11.2g | |
| D. | 原混合物中CuO与Fe2O3的质量比为1:2 |


