题目内容
Ⅰ.科学家经过多年研究证明,很多同学爱吃的某些小包装零食中,含一定量的有毒、有害、致病的化学物质,如某些油炸食品中含有致癌物质丙烯酰胺,丙烯酰胺的化学式为C3H5ON.回答下列问题(1)每个丙烯酰胺分子中有 个原子.
(2)丙烯酰胺中碳元素的质量分数是 (保留一位小数).
Ⅱ.近来有科学家提出利用“碳捕捉技术”来降低工业生产中二氧化碳的排放量.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用足量的NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).
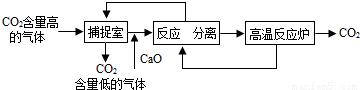
(1)捕捉室中发生反应的化学方程式为: ;
(2)把CaO放入反应分离室中与H2O反应,请写出该反应的化学方程式: ;利用此反应,氧化钙可用作食品 剂;
(3)“反应分离”中为将固体和液体分离,所用到的基本操作是 ,该固体是碳酸钙.
(4)整个过程中,可以循环利用的物质是 和 .
【答案】分析:Ⅰ、(1)依据丙烯酰胺的化学式回答;
(2)依据元素的质量分数计算方法进行解答;
Ⅱ、根据二氧化碳与氢氧化钠反应的反应物、生成物写出化学方程式;生石灰可与水反应,故可作干燥剂;过滤是将固体和液体分离的方法,据流程图分析可循环利用的物质.
解答:解:Ⅰ、(1)丙烯酰胺的化学式为C3H5ON,由此可知每个丙烯酰胺分子中有10个原子;
(2)丙烯酰胺中碳元素的质量分数是 ×100%≈50.7%;
×100%≈50.7%;
Ⅱ、(1)捕捉室中发生反应的化学反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,化学方程式为CO2+2NaOH═Na2CO3+H2O;
(2)CaO和水反应生成氢氧化钙,因此氧化钙可以做干燥剂;
(3)固体与液体分开用过滤;
(4)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;碳酸钙高温生成氧化钙和二氧化碳,观察图示,氧化钙还可循环利用,氧化钙和氢氧化钠都可以循环利用;
故答案为:Ⅰ.(1)10; (2)50.7%;
Ⅱ.(1)CO2+2NaOH═Na2CO3+H2O;
(2)CaO+H2O═Ca(OH)2;干燥剂;
(3)过滤;
(4)氢氧化钠、氧化钙.
点评:本题考查了分子构成、元素的质量分数及对物质的性质和流程图的分析,注重对学生解读解能力的考查,有利于培养学生的探究能力.
(2)依据元素的质量分数计算方法进行解答;
Ⅱ、根据二氧化碳与氢氧化钠反应的反应物、生成物写出化学方程式;生石灰可与水反应,故可作干燥剂;过滤是将固体和液体分离的方法,据流程图分析可循环利用的物质.
解答:解:Ⅰ、(1)丙烯酰胺的化学式为C3H5ON,由此可知每个丙烯酰胺分子中有10个原子;
(2)丙烯酰胺中碳元素的质量分数是
 ×100%≈50.7%;
×100%≈50.7%;Ⅱ、(1)捕捉室中发生反应的化学反应是二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,化学方程式为CO2+2NaOH═Na2CO3+H2O;
(2)CaO和水反应生成氢氧化钙,因此氧化钙可以做干燥剂;
(3)固体与液体分开用过滤;
(4)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠又是捕捉室中的反应物,所以可以循环利用;碳酸钙高温生成氧化钙和二氧化碳,观察图示,氧化钙还可循环利用,氧化钙和氢氧化钠都可以循环利用;
故答案为:Ⅰ.(1)10; (2)50.7%;
Ⅱ.(1)CO2+2NaOH═Na2CO3+H2O;
(2)CaO+H2O═Ca(OH)2;干燥剂;
(3)过滤;
(4)氢氧化钠、氧化钙.
点评:本题考查了分子构成、元素的质量分数及对物质的性质和流程图的分析,注重对学生解读解能力的考查,有利于培养学生的探究能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 科学家经过多年研究证明,某些零食中含一定量的有害物质,如油炸食品中常含有致癌物质丙烯酰胺(C3H5NO).
科学家经过多年研究证明,某些零食中含一定量的有害物质,如油炸食品中常含有致癌物质丙烯酰胺(C3H5NO).