题目内容
1.为测定23g某氯化钠和碳酸钠固体混合物中碳酸钠的含量,如图所示,加入一定量的氯化钡溶液至恰好完全反应,经过一系列操作后得到固体25.2g.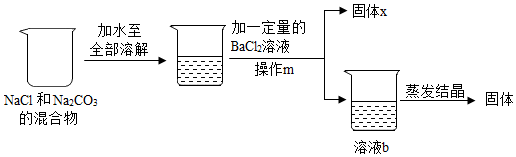
(1)操作m需要用到的仪器有铁架台、漏斗、烧杯、玻璃棒等;
(2)计算该固体中碳酸钠的质量分数(最后结果保留0.1%)
分析 (1)过滤可以将固体和液体分开;
(2)向碳酸钠和氯化钠组成的混合溶液中加入氯化钡溶液,碳酸钠与氯化钡发生反应生成碳酸钡沉淀和氯化钠,而混合溶液中的氯化钠不与氯化钡反应;至恰好完全反应后,所得溶液为氯化钠溶液,其溶质氯化钠由两部分组成:一部分为原混合物质中的氯化钠,另一部分则是反应生成的氯化钠;可以根据物质质量的增加结合方程式计算碳酸钠的质量,进一步计算该固体中碳酸钠的质量分数.
解答 解:(1)图中将固体和液体分开的操作为过滤,过滤需要用到的仪器有铁架台、漏斗、烧杯、玻璃棒等.故填:铁架台、漏斗、烧杯、玻璃棒等;
(2)设固体混合物中Na2CO3的质量为x,
Na2CO3+BaCl2═BaCO3↓+2NaCl 质量增加
106 117 117-106=11
x 25.2g-23g=2.2g
$\frac{106}{x}=\frac{11}{2.2g}$
x=21.2g
该固体中碳酸钠的质量分数$\frac{21.2g}{23g}×100%$=92.2%.
答:该固体中碳酸钠的质量分数92.2%.
点评 本题考查学生利用量差法解题,能够找出反应前后的质量关系是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.某化学兴趣小组同学对家用普通干电池中含有的物质产生了浓厚的兴趣.他们剥开电池时闻到氨味且发现有黑色物质.
【提出问题】为什么有氨味?黑色物质的成分是什么?
【猜想假设】能闻到氨味说明含有铵盐(如NH4Cl);黑色固体可能有铁粉、氧化铜或二氧化锰.
【实验探究】同学们分别设计实验进行探究.
实验I.小聪取适量黑色物质与熟石灰混合置于研钵内研磨,嗅到强烈氨味,再用湿润的红色石蕊试纸检测,观察到试纸变蓝,证明黑色物质中含有铵盐.
实验II.小敏将黑色物质加入适量的水中搅拌溶解,静置后过滤,取不溶物进行实验.
【交流讨论】
步骤2中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
【提出问题】为什么有氨味?黑色物质的成分是什么?
【猜想假设】能闻到氨味说明含有铵盐(如NH4Cl);黑色固体可能有铁粉、氧化铜或二氧化锰.
【实验探究】同学们分别设计实验进行探究.
实验I.小聪取适量黑色物质与熟石灰混合置于研钵内研磨,嗅到强烈氨味,再用湿润的红色石蕊试纸检测,观察到试纸变蓝,证明黑色物质中含有铵盐.
实验II.小敏将黑色物质加入适量的水中搅拌溶解,静置后过滤,取不溶物进行实验.
| 实验步骤 | 实验现象.实验结论 | |
| 1、取适量黑色滤渣装入试管中,再加入过量稀盐酸 | 无气泡生成,溶液不变色 | 黑色粉末中一定不含铁粉与氧化铜 |
| 2、取适量黑色滤渣装入另一支试管中,再加入H2O2(或过氧化氢)溶液,向上述试管中伸入带火星的小木条. | 木条复燃 | 黑色粉末中含有二氧化锰 |
步骤2中发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
9.下列事实与解释相符的是( )
| A. | 干冰用作制冷剂--干冰是冰 | |
| B. | 酸雨是PH<5.6的雨水--二氧化碳是形成酸雨的主要气体 | |
| C. | 用炭黑墨汁书写的字经久不变色--常温下,碳的化学性质稳定 | |
| D. | 制糖工业用活性炭脱色制白糖--活性炭和有色物质反应 |
16.馒头、面包等发面食品的一个特点是面团中有许多小孔,他们使发面食品松软可口.小明学习相关化学知识后,将家里制作馒头用的白色粉末带到实验室与兴趣小组的同学一起进行探究.
【初步探究】取少量白色粉末于试管中,加适量水,测得溶液的 pH>7,说明溶液呈碱性.
【提出问题】白色粉末成分是什么?
【查阅资料】
(1)碳酸钠、碳酸氢钠都可用于制作发面食品.
(2)碳酸氢钠不稳定,受热易分解生成二氧化碳和水等; 碳酸钠很稳定.
【猜想与假设】
猜想Ⅰ:碳酸钠
猜想Ⅱ:碳酸氢钠
【实验探究】甲乙兴趣小组设计不同实验方案进行探究.
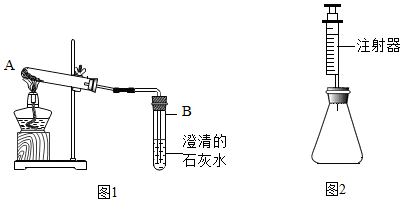
甲组方案:如图1,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想Ⅱ正确.写出装置B中反应的化学方程式CO2+Ca(OH)2══CaCO3↓+H2O.
乙组方案:用如图2所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分.
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
实验①的化学反应方程式为Na2CO3+2HCl══2NaCl+CO2↑+H2O; 表中 m=ag; 根据上表中数据分析,猜想Ⅱ正确,判断的依据是V3=V2.
【反思应用】
(1)甲组方案中,无法判断白色粉末是否为碳酸钠和碳酸氢钠的混合物;乙组方案可以判断,如果是两者的混合物,应该满足的条件是V1<V3<V2.
(2)家中制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢钠,可以使馒头、面包松软.原因是碳酸氢钠与有机酸反应生成二氧化碳气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔.
【初步探究】取少量白色粉末于试管中,加适量水,测得溶液的 pH>7,说明溶液呈碱性.
【提出问题】白色粉末成分是什么?
【查阅资料】
(1)碳酸钠、碳酸氢钠都可用于制作发面食品.
(2)碳酸氢钠不稳定,受热易分解生成二氧化碳和水等; 碳酸钠很稳定.
【猜想与假设】
猜想Ⅰ:碳酸钠
猜想Ⅱ:碳酸氢钠
【实验探究】甲乙兴趣小组设计不同实验方案进行探究.

甲组方案:如图1,取适量白色粉末于试管中,将导管伸入澄清石灰水,加热,澄清石灰水变浑浊,猜想Ⅱ正确.写出装置B中反应的化学方程式CO2+Ca(OH)2══CaCO3↓+H2O.
乙组方案:用如图2所示装置作为反应容器,准确测量生成气体的体积以判断白色粉末的成分.
分别向盛有碳酸钠、碳酸氢钠和白色粉末的锥形瓶中,注入等体积、等浓度的足量的稀盐酸,记录如表:
| 实验编号 | 锥形瓶内物质[来源 | 最终得到 CO2 体积/mL | |
| 名称 | 质量/g | ||
| ① | 碳酸钠 | a | V1 |
| ② | 碳酸氢钠 | a | V2 |
| ③ | 白色粉末 | m | V3 |
【反思应用】
(1)甲组方案中,无法判断白色粉末是否为碳酸钠和碳酸氢钠的混合物;乙组方案可以判断,如果是两者的混合物,应该满足的条件是V1<V3<V2.
(2)家中制作馒头、面包时,将面粉发酵(产生有机酸),再加入适量的碳酸氢钠,可以使馒头、面包松软.原因是碳酸氢钠与有机酸反应生成二氧化碳气体,气体在面团中形成许多小气室,使馒头、面包疏松多孔.
13.下列各组离子在pH值为14的某溶液中能大量共存的是( )
| A. | Ba2+,、K +,、SO42-、NO3 - | B. | Ca2+、Al3+、Cl-、NO3- | ||
| C. | K+、Na+、SO42-、CO32- | D. | NH4+、Na+、SO42-、NO3- |
10.保护环境,节约资源,从我做起.下列做法不符合这一理念的是( )
| A. | 使用降解塑料 | B. | 推广乙醇汽油 | ||
| C. | 废旧电池掩埋在土壤中 | D. | 减少燃煤使用 |