题目内容
6.将“天舟一号”空间实验室送入太空的是“长征二号”F运载火箭,有关问题如下:(1)火箭用联氨(N2H4)做燃料,用四氧化二氮(N2O4)助燃,生成物不会对大气造成污染.
①完成燃烧反应的化学方程式:2N2H4+N2O4=3N2+4H2O.
②通过此反应谈谈你对燃烧有什么新的认识?燃烧不一定需要氧气.
③N2O4中的氮元素的化合价是+4价.四氧化二氮常温下就能转化成二氧化氮(NO2),NO2与N2O4比较,不同点是.B
A.氮元素的化合价 B.分子中原子的个数 C.物质中氮元素的质量分数 D.组成元素
(2)载人航天飞行器的模拟座中,空气更新过程如下图所示.
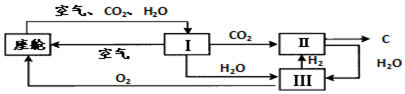
①装置Ⅰ的作用是分离空气、CO2和H2O.
②在装置Ⅰ、Ⅱ、Ⅲ中发生化学变化的是Ⅱ、Ⅲ(填序号).
③从装置Ⅰ、Ⅱ、Ⅲ可看出,O2的来源是CO2和H2O,若产生800g O2,消耗880g CO2,则同时消耗H2O180g.
分析 (1)①根据化学变化前后原子的种类不变、原子个数没有增减,推断反应物所空物质的化学式;②根据燃烧概念分析.③利用两物质的化学式NO2与N2O4,分别计算氮元素的化合价、氮元素的质量分数及相对分子质量,判断组成元素与分子中原子的个数;选出其中不同的选项.
解答 解:(1)①根据质量守恒定律,化学反应前后原子的个数不变,反应前反应物中N、H、O元素的原子个数依次为:6、8、4,反应后生成物中H、O原子个数为8、4;比较反应前后原子种类及个数可得知,3个未知物的分子中应含有6个N原子,所以,未知物的化学式为N2;
②由联氨燃烧可知,此反应是燃烧反应,却没有氧气的参与,故可得出,燃烧不一定需要氧气;
③根据两物质的化学式NO2与N2O4,可得知两物质都由N、O两种元素组成且其中N、O原子个数比相等都为1:2,则两物质中氮元素的化合价、氮元素的质量分数也相等;物质NO2的分子中含3个原子而物质N2O4的分子中含有6个原子;故选B;
(2)①根据装置I提供水和二氧化碳,装置I是为了分离空气、水和二氧化碳,为装置Ⅱ、Ⅲ提供二氧化碳和水;
②由图可知,发生化学变化的是Ⅱ和Ⅲ,分别是:Ⅱ中发生反应的化学方程式为:CO2+2H2=C+2H2O;装置Ⅲ中只有水,水电解的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
③消耗880g CO2产生的氧气质量为:880g×$\frac{32}{44}×100%$=640g,
则同时消耗H2O的质量为:(800g-640g)÷$\frac{16}{18}×100%$=180g;
故答案为:(1)①N2;②燃烧不一定需要氧气;③B;(2)①分离空气、CO2和H2O;②Ⅱ、Ⅲ;③180.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案| A. | 氢氧化钠可用于治疗胃酸过多症 | |
| B. | 工业上一般用焦炭、石灰石和铁矿石炼铁 | |
| C. | 金刚石的硬度大可用于切割玻璃 | |
| D. | 氮气的化学性质不活泼,常用作保护气 |
| A. | 红磷在空气中燃烧,产生大量的白雾 | |
| B. | 铁丝浸入稀盐酸,形成黄色溶液 | |
| C. | 持续加热碳酸氢钠,最终没有固体残留 | |
| D. | 向氢氧化钠溶液中加入硫酸铜溶液有蓝色沉淀生成 |
| 物质 | A | B | C | D | 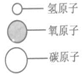 |
| 分子示意图 | ? |  |  |  |
(2)反应过程中A物质与B物质的质量比为11:40.
| A. | 服用含氢氧化铝的药物治疗胃酸过多 Al(OH)3+3HCl=AlCl3+3H2O 复分解反应 | |
| B. | 不能用铁桶盛放波尔多液 Fe+CuSO4=Cu+FeSO4 分解反应 | |
| C. | 用天然气作燃料 CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 验证铜和铝的活动性 3Cu+A12(SO)3=3CuSO+2Al 置换反应 |
| A. | 回收输液器再利用,做成食品塑料袋 | |
| B. | 推广无纸化办公,使用再生纸且双面打印 | |
| C. | 大力发展新资源,禁止使用化石燃料 | |
| D. | 把废水利用高压泵打入地下,减少对河流污水的排放 |
 (1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.
(1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.