题目内容
5. 某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示.则下列关于溶液中溶质的判断正确的是( )
某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液中的一种或几种混合形成,现向该混合溶液中滴入氢氧化钡溶液,产生沉淀的质量与加入氢氧化钡溶液体积的关系如图所示.则下列关于溶液中溶质的判断正确的是( )| A. | 可能含有碳酸钠 | |
| B. | 肯定没有硫酸 | |
| C. | 是否含有氯化铜不能确定 | |
| D. | 至少含有硫酸或盐酸中的一种,也可能两种同时含有 |
分析 某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液中的一种或几种混合形成,根据盐酸和硫酸分别都可以和碳酸钠溶液反应,所以不能存在硫酸和碳酸钠混合物,也不会是盐酸和碳酸钠溶液的混合物.同时由于碳酸钠和氯化铜能够生成碳酸铜不溶性物质,所以也不存是这两者的混合物.向该混合溶液中滴入氢氧化钡溶液,根据图中可以看出,起始阶段没有沉淀产生沉淀,所以混合物中不含有硫酸根离子,由于消耗了氢氧化钡,所以一定存在盐酸,所以一定不存在碳酸钠.由于盐酸和氢氧化钡反应逐渐消耗,直至盐酸被完全消耗,才产生沉淀,所以该沉淀一定不是硫酸钡或者碳酸钡.由于加入的是氢氧化钡,所以对应的沉淀应该是与氢氧根离子有关,所以生成的沉淀物为氢氧化铜沉淀.所以原混合物应该为盐酸和氯化铜的混合物.
解答 解:某溶液由盐酸、碳酸钠溶液、稀硫酸、氯化铜溶液中的一种或几种混合形成,根据盐酸和硫酸分别都可以和碳酸钠溶液反应,所以不能存在硫酸和碳酸钠混合物,也不会是盐酸和碳酸钠溶液的混合物.同时由于碳酸钠和氯化铜能够生成碳酸铜不溶性物质,所以也不存是这两者的混合物.向该混合溶液中滴入氢氧化钡溶液,根据图中可以看出,起始阶段没有沉淀产生沉淀,所以混合物中不含有硫酸根离子,由于消耗了氢氧化钡,所以一定存在盐酸,所以一定不存在碳酸钠.由于盐酸和氢氧化钡反应逐渐消耗,直至盐酸被完全消耗,才产生沉淀,所以该沉淀一定不是硫酸钡或者碳酸钡.由于加入的是氢氧化钡,所以对应的沉淀应该是与氢氧根离子有关,所以生成的沉淀物为氢氧化铜沉淀.所以原混合物应该为盐酸和氯化铜的混合物.
A、由上述分析可知,溶液中含有盐酸,一定不含有碳酸钠,故A错误.
B、由于加入氢氧化钡后,不是从加入时就产生沉淀,所以一定不含硫酸.故B正确
C、由于开始加入氢氧化钡没有沉淀,所以沉淀应该是氢氧根离子有关的氢氧化铜沉淀,所以一定含有氯化铜.错误.
D、根据B分析,一定不存在硫酸,所以也就不存在两者共存的可能.错误.
故选:B.
点评 图表分析时一定要注意从图中归纳出信息提示,如本题中加入氢氧化钡,却在开始阶段没有沉淀,所以硫酸根离子存在,而同时消耗了氢氧化钡,所以该混合物一定能够消耗氢氧根离子,所以混合物为酸性的溶液.

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案| A. | 牛奶变质;石油分馏 | |
| B. | 汽油挥发;用盐酸除铁锈 | |
| C. | 生石灰遇水放热;镁带在空气中燃烧后变为白色粉末 | |
| D. | 用木炭除去冰箱中的异味;给水通直流电 |
| 序号 | 物 质 | 杂 质 | 除杂质应选用的试剂或操作方法 |
| ① | Cu | Fe | 加入足量稀盐酸,充分反应后,过滤、洗涤、干燥 |
| ② | 氮气 | 氧气 | 通过足量的灼热的铜网 |
| ③ | CO2 | HCl、H2O | 依次通过盛有足量饱和NaHCO3溶液和浓硫酸的洗气瓶 |
| ④ | NaCl溶液 | CaCl2、MgCl2、Na2SO4 | 依次加入过量的BaCl2溶液、Na2CO3溶液、NaOH溶液,充分反应后过滤,再滴加稀盐酸调节溶液pH为7 |
| A. | ①②③④ | B. | ②③④ | C. | ③④ | D. | ①②④ |
(1)他们依据所学的化学知识,对烧杯内溶液中的溶质的成分作了如下猜想:
①可能是CaCl2; ②CaCl2与和Ca(OH)2; ③可能是CaCl2与和HCl组成的混合溶液
小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液.振荡.观察到酚酞试液不变色.于是他排除了猜想②,
小花想用碳酸钠溶液来验证剩下的两种猜想,请你帮她完成实验,填写以下表格:
| 实验步骤 | 预计现象 | 预计结论 |
| 取少量反应后的溶液于试管中,逐滴加入碳酸钠溶液. | 猜想①正确 | |
| 猜想③正确 |
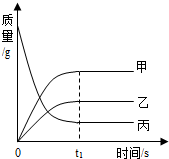 如图反映了某个化学反应各物质质量与时间的关系.
如图反映了某个化学反应各物质质量与时间的关系.
 知某混合物中只含Na2CO3和NaOH.现取该样品26.2g,逐滴加入稀盐酸,生成的二氧化碳与滴加的稀盐酸的质量关系如图所示:
知某混合物中只含Na2CO3和NaOH.现取该样品26.2g,逐滴加入稀盐酸,生成的二氧化碳与滴加的稀盐酸的质量关系如图所示: