题目内容
15.量取一定体积的液体应用量筒,选择的量筒规格与所量液体体积越接近越好.倾倒的液体接近刻度时,应用胶头滴管滴加.量液时,量筒必须放平,视线要与量筒内液体凹液面最低处保持水平再读出读数.仰视时会造成读数偏偏小,俯视时会造成读数偏偏大,胶头滴管的使用方法:取液后的滴管,应保持胶帽在上,不要平放或倒置,防止液体倒流,玷污试剂或腐蚀胶帽;滴加时把滴管放在容器口上方滴加.用过的滴管要立刻用清水冲洗干净(滴瓶上的滴管不要用水冲洗)分析 根据液体药品的取用方法和注意事项进行分析解答.
解答 解:取用一定量的液体常用量筒.选择的量筒规格与所量液体体积越接近越好.倾倒的液体接近刻度时,应用胶头滴管滴加.量液时,量筒必须放平,视线要与量筒内液体凹液面最低处保持水平再读出读数.仰视时会造成读数偏偏小,俯视读数导致读数结果偏大;胶头滴管的使用方法:取液后的滴管,应保持橡胶头在上,不要平放或倒置,防止液体倒流,玷污试剂或腐蚀橡胶帽腐蚀橡胶头;滴加时把滴管放在容器口上方滴加.用过的滴管要立刻用清水冲洗干净(滴瓶上的滴管不要用水冲洗).
故答案为:量筒;胶头滴管;放平;凹液面的最低处;偏小;偏大;胶帽;试剂;胶帽;清水冲洗.
点评 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
20.如图所示,这四位同学描述的可能是下面的同一个化学符号( )


| A. | CO2 | B. | O2 | C. | NO | D. | HClO |
4.化学改变世界的途径是使物质发生化学变化.下列属于化学变化的是( )
| A. | 冰块制成冰雕 | B. | 钨丝灯泡发光放热 | ||
| C. | 泥土烧成瓷器 | D. | 工业上从空气中分离出氧气 |
5.如图是元素周期表中的一种元素,下列有关该元素的信息正确的是( )


| A. | 原子序数是16 | B. | 它是金属元素 | ||
| C. | 核内质子数是32 | D. | 相对原子质量是16 |
 某同学用空塑料饮料瓶作简易净水器,设计如图,请你帮助他继续设计:
某同学用空塑料饮料瓶作简易净水器,设计如图,请你帮助他继续设计: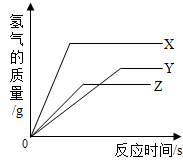 为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的同一种稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )
为探究X、Y、Z三种金属与酸的反应情况,进行了如下实验:取等质量的X、Y、Z分别与足量的同一种稀硫酸反应,都生成+2价金属的硫酸盐,反应情况如图所示.下列对该图象理解的叙述中,正确的是( )

 如图是电解水的简易装置:
如图是电解水的简易装置: