题目内容
13.用硝酸钠固体配制100g 5%的硝酸钠溶液,应选用的一组仪器是( )| A. | 托盘天平、烧杯、玻璃棒、10 mL量筒 | |
| B. | 托盘天平、烧杯、玻璃棒、100 mL量筒 | |
| C. | 托盘天平、烧杯、铁架台、10 mL量筒 | |
| D. | 托盘天平、烧杯、100 mL量筒 |
分析 实验室配制100g 5%的硝酸钠溶液操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要.
解答 解:溶质质量=溶液质量×溶质的质量分数,配制100g溶质质量分数为5%的硝酸钠溶液,需硝酸钠的质量=100g×5%=5g;溶剂质量=溶液质量-溶质质量,所需水的质量为100g-5g=95g(合95mL),量筒量程选择的依据有两点:一是保证量取一次,二是量程与液体的取用量最接近,应用100mL量筒量取95mL水;托盘天平用于称取固体硝酸钠、100mL的量筒用于准确量取水、烧杯用于完成溶解操作、玻璃棒用于溶解时的搅拌.
A、不能使用10mL量筒,故选项错误.
B、配制100g 5%的硝酸钠溶液,可使用托盘天平、烧杯、玻璃棒、100 mL量筒,故选项正确.
C、配制溶液的过程中不需要使用铁架台,不能使用10mL量筒,故选项错误.
D、配制溶液的过程中需要使用玻璃棒进行引流,选项中缺少玻璃棒,故选项错误.
故选:B.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
3.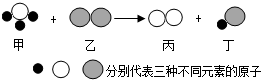 如图是某反应的微观示意图,对该图示描述错误的是( )
如图是某反应的微观示意图,对该图示描述错误的是( )
 如图是某反应的微观示意图,对该图示描述错误的是( )
如图是某反应的微观示意图,对该图示描述错误的是( )| A. | 该反应前后元素的种类没变 | |
| B. | 生成物丁可能是氧化物 | |
| C. | 该反应属于分解反应 | |
| D. | 该反应中甲物质的一个分子中含有四个原子. |
1.2012年3月15日起,我国各地开始实施新的碘盐含碘量标准.已知,目前山西省碘盐中的含碘量标准为25mg/kg,这里的“碘”是指( )
| A. | 碘原子 | B. | 碘元素 | C. | 碘分子 | D. | 碘单质 |
18.一密闭容器中有甲、乙、丙、丁四种物质,在一定的条件下充分反应,测得反应前后各物质质量如下表:
反应后,甲的“待测”值应为( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 1 | 42 | 10 |
| 反应后质量(g) | 待测 | 20 | 6 | 31 |
| A. | 10 | B. | 8 | C. | 4 | D. | 0 |
5.化学方程式配平后的特征是( )
| A. | 方程式前后各物质的质量相等 | |
| B. | 方程式前后各化学式的化学计量数之和相等 | |
| C. | 方程式前后分子种类相同 | |
| D. | 方程式前后各元素的原子个数相等 |
3.在25℃时,向不饱和氯化钾溶液中加入少量氯化钾固体至溶液刚好饱和,在这一过程中,下列各量中不变的是( )
| A. | 溶剂的质量 | B. | 溶质的质量 | ||
| C. | 溶液的溶质质量分数 | D. | 溶液的质量 |




