题目内容
2. 如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答:
如图是a、b、c三种物质(均不含结晶水)的溶解度曲线,请你回答:(1)0℃时,a、b、c三种物质中溶解度最大的是C;
(2)t2℃,将a、b、c三种物质的饱和溶液降温至0℃,析出晶体
最多的是a;
(3)若a中混有少量b,提纯a的方法是降温结晶;
(4)要使接近饱和的a溶液变为饱和溶液,可采取的方法是加入a物质(填1种)加入a物质
(5)t2℃a的饱和溶液中溶质的质量分数是33.3%.
分析 (1)根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
(2)根据a、b、c三种物质的溶解度曲线,分析溶解度随温度变化的情况,判断在降温时析出晶体的多少;
(3)根据a的溶解度随温度的升高而增大解答;
(4)根据饱和溶液和不饱和溶液之间可以相互转化解答;
(5)根据饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%解答.
解答 解:(1)0℃时,三种物质的溶解度大小关系是c>b>a.
(2)由A、B、C三种物质的溶解度曲线可知,a、b的溶解度随温度的升高而增大,C的变化幅度最大,c的随温度的升高而减小.t2℃,将a、b、c三种物质的饱和溶液降温至0℃,析出晶体最多的是a,c没有晶体析出;
(3)a的溶解度随温度的升高而增大,若a中混有少量b,提纯a的方法是降温结晶;
(4)要使接近饱和的a溶液变为饱和溶液,可采用的方法有:加入a物质,降低温度,恒温蒸发溶剂等.
(5)t2℃a的溶解度是50g,t2℃a的饱和溶液中溶质的质量分数是$\frac{50g}{100g+50g}×$100%≈33.3%
答案:
(1)c;
(2)a;
(3)降温结晶;
(4)加入a物质;
(5)33.3%.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.CO2在高温下能与木炭反应生成CO.为验证该反应,某课外兴趣小组设计了一套实验装置,装置图如图所示(夹持装置及加热部分未画出):

(1)根据装置图,填写如表:
(2)D处要增加的仪器名称是酒精灯.
(3)写出CO2在高温下与木炭反应生成CO的化学方程式CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(4)验证CO的方法是点燃气体,火焰呈蓝色,再用内壁附着有澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊.

(1)根据装置图,填写如表:
| 仪器标号 | 仪器中所加物质 | 作 用 |
| A | 石灰石,稀盐酸 | 石灰石与盐酸作用产生CO2 |
| B | 饱和碳酸氢钠溶液(与CO2不反应) | 除去CO2中的HCl气体 |
| C | 浓硫酸 | 干燥CO2气体 |
| D | 干燥的木炭粉 | 与CO2反应生成CO |
| E | 澄清石灰水(或Na0H溶液) | 吸收未反应的CO2 |
(3)写出CO2在高温下与木炭反应生成CO的化学方程式CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO.
(4)验证CO的方法是点燃气体,火焰呈蓝色,再用内壁附着有澄清石灰水的烧杯罩在火焰上,烧杯内壁的石灰水变浑浊.
12.2015年11月2日,C919大型客机首架机正式下线.制造大飞机使用了大量的铝、铁、铜.小组同学对三种金属进行了如下探究:
【实验】
【分析】(1)实验时,需先用砂纸打磨金属片,其目的是除去金属表面的氧化膜,利于反应.
(2)如果要验证铝、铁、铜三种金属活动性强弱,从优化实验的角度考虑,只需利用上述实验中的BE(用实验编号填空)两组实验就能达到目的.
(3)将打磨后的铝片放入稀硫酸中,开始反应很慢,然后试管逐渐变热,反应逐渐加快.一段时间后,反应速率变慢,最后停止产生气泡.请结合所学知识,解释产生该现象的原因铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜.将铝条放入稀盐酸中,稀盐酸与铝条表面的氧化铝反应,所以气泡较少.随着氧化铝的减少,铝与盐酸接触面积增大,气泡逐渐增加并达到反应最快.后来盐酸的质量分数越来越小,反应速率减慢.直至停止.
【拓展】将一定质量的锌粉加入含硝酸铝、硝酸铜和硝酸银的溶液中,充分反应后过滤,然后分别向滤液、滤渣中加入稀盐酸,均无明显现象,则滤液中存在的阳离子可能是Al3+、Zn2+或Al3+、Zn2+、Cu2+或Al3+、Zn2+、Cu、Ag+(用离子符号表示所有可能存在的情况).
【实验】
| 实验 | 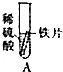 | 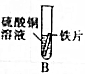 | 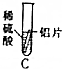 | 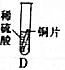 |  |
| 现象 | 有气泡产生,产生气泡较慢 | 铁片上有红色物质附着,溶液变成浅绿色 | 有气泡产生,产生气泡较快 | 无现象 | 无气泡产生无明显现象 |
(2)如果要验证铝、铁、铜三种金属活动性强弱,从优化实验的角度考虑,只需利用上述实验中的BE(用实验编号填空)两组实验就能达到目的.
(3)将打磨后的铝片放入稀硫酸中,开始反应很慢,然后试管逐渐变热,反应逐渐加快.一段时间后,反应速率变慢,最后停止产生气泡.请结合所学知识,解释产生该现象的原因铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜铝易被空气中的氧气氧化,在铝条表面生成一层致密的氧化物保护膜.将铝条放入稀盐酸中,稀盐酸与铝条表面的氧化铝反应,所以气泡较少.随着氧化铝的减少,铝与盐酸接触面积增大,气泡逐渐增加并达到反应最快.后来盐酸的质量分数越来越小,反应速率减慢.直至停止.
【拓展】将一定质量的锌粉加入含硝酸铝、硝酸铜和硝酸银的溶液中,充分反应后过滤,然后分别向滤液、滤渣中加入稀盐酸,均无明显现象,则滤液中存在的阳离子可能是Al3+、Zn2+或Al3+、Zn2+、Cu2+或Al3+、Zn2+、Cu、Ag+(用离子符号表示所有可能存在的情况).
10.点燃H2、O2、N2的混合气体40g,完全反应后生成36g水,则剩余的气体不可能的是(提示:H2和O2在点燃的条件下,生成水,在此反应过程中,N2不参加反应)
| A. | H2、O2、N2的混合气体 | B. | O2和N2的混合气体 | ||
| C. | H2和N2的混合气体 | D. | 4gN2 |
17.“盐巴”即食盐,因古代巴人熬制垄断食盐销售而得名.下列说法错误的是( )
| A. | 海水、盐矿都是“盐巴”的重要来源 | |
| B. | 因人体代谢原因,每天需补充大量“盐巴” | |
| C. | 熬制“盐巴”利用了蒸发结晶原理 | |
| D. | “盐巴”可制取纯碱、烧碱等多种化工产品 |
7.2015年9月20日7时01分,中国在太原卫星发射中心用全新研制的长征六号运载火箭,成功将20颗卫星发射升空,卫星顺利进入预定轨道,开创了我国一箭多星发射的新纪录.为提高火箭的运载能力,新型火箭使用的燃料为液氧煤油,液氧煤油燃烧时主要发生的反应的化学方程式为:X+14O2$\frac{\underline{\;点燃\;}}{\;}$9CO2+10H2O,X的化学式为( )
| A. | CH4 | B. | C2H8 | C. | C9H20 | D. | C10H20 |
11.最初输水管材用铸铁,目前多用塑料管,输送热水一般用铜管.
(1)下列管材不属于金属材料的是AB(填字母序号).
(2)铁锅、铝锅、铜锅用来炒菜、做饭是利用了它们的C(填字母序号).
A.导电性 B.延展性 C.导热性 D.有金属光泽.
(1)下列管材不属于金属材料的是AB(填字母序号).
 |  |  |
| A.铸铁管 | B.铜管 | C.塑料管 |
A.导电性 B.延展性 C.导热性 D.有金属光泽.