题目内容
19. 元素周期表中硒元素的某些信息如图所示,下列有关硒的说法不正确的是( )
元素周期表中硒元素的某些信息如图所示,下列有关硒的说法不正确的是( )| A. | 原子核内有34个质子 | B. | 硒元素是金属元素 | ||
| C. | 相对原子质量为78.96 | D. | 缺硒可能引起表皮角质化和癌症 |
分析 根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,当质子数=核外电子数,为原子;进行分析判断即可.
解答 解:A.根据元素周期表中的一格中获取的信息,该元素的原子序数为34,因此核外电子数=原子序数=34;故选项说法正确.
B.根据元素周期表中的一格中获取的信息,该元素的名称是硒,属于非金属元素,故选项说法错误.
C.根据元素周期表中的一格中获取的信息,可知元素的相对原子质量为78.96,故选项说法正确.
D.硒有防癌、抗癌作用,缺硒可能引起表皮角质化和癌症,故选项说法正确.
故选:B.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、化学元素与人体健康的关系进行分析解题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列图示与对应的叙述相符的是( )
| A. | 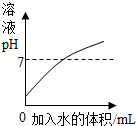 表示向稀盐酸中不断加水 表示向稀盐酸中不断加水 | |
| B. |  表示探究过氧化氢制氧气的反应中二氧化锰的作用 表示探究过氧化氢制氧气的反应中二氧化锰的作用 | |
| C. | 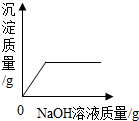 表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 表示向盐酸和氯化镁的混合溶液中滴加氢氧化钠溶液 | |
| D. | 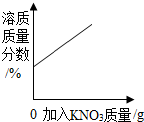 表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体 表示20℃时,向一定量的接近饱和的硝酸钾溶液中加入硝酸钾固体 |
8.我国青海湖采集的天然碱样品可表示为aNa2CO3•bNaHCO3•cH2O(a、b、c为最简整数比).小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:

已知:
1.碳酸钠比较稳定,加热不分解;
2.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤
(1)实验时,组装好装置,实验前应先检查装置气密性,后续实验步骤是:
①反复推拉注射器 ②称量E、F的质量 ③关闭弹簧夹,加热D处试管直到反应不再进行 ④打开弹簧夹,再次反复缓缓推拉注射器 ⑤再次称量E、F的质量.
(二)问题探究:
(2)E中的药品为浓硫酸,E的作用是吸收水蒸气.
实验过程中,C的作用是除去空气中的水蒸气和二氧化碳,F的作用是吸收反应生成的二氧化碳.
写出 F装置中所发生反应的一个化学方程式CO2+2NaOH═Na2CO3+H2O.
(3)实验步骤②与③能否颠倒不能(填“能”或“不能”).若不进行步④的操作,则所测得的碳酸氢钠质量偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是防止气体流速太快,来不及被吸收;若没有G装置,则碳酸氢钠的质量偏大(填“偏大”、“偏小”、“无影响”).
(4)下表是实验记录数据:
则:①碳酸氢钠分解生成二氧化碳的质量为1.1g
②碳酸氢钠的质量为4.2g
③该天然碱的化学式中a:b:c=2:1:2.

已知:
1.碳酸钠比较稳定,加热不分解;
2.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2↑+H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤
(1)实验时,组装好装置,实验前应先检查装置气密性,后续实验步骤是:
①反复推拉注射器 ②称量E、F的质量 ③关闭弹簧夹,加热D处试管直到反应不再进行 ④打开弹簧夹,再次反复缓缓推拉注射器 ⑤再次称量E、F的质量.
(二)问题探究:
(2)E中的药品为浓硫酸,E的作用是吸收水蒸气.
实验过程中,C的作用是除去空气中的水蒸气和二氧化碳,F的作用是吸收反应生成的二氧化碳.
写出 F装置中所发生反应的一个化学方程式CO2+2NaOH═Na2CO3+H2O.
(3)实验步骤②与③能否颠倒不能(填“能”或“不能”).若不进行步④的操作,则所测得的碳酸氢钠质量偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是防止气体流速太快,来不及被吸收;若没有G装置,则碳酸氢钠的质量偏大(填“偏大”、“偏小”、“无影响”).
(4)下表是实验记录数据:
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为102.25g |
| F的质量为50.0g | F的质量为51.1g |
②碳酸氢钠的质量为4.2g
③该天然碱的化学式中a:b:c=2:1:2.
 已知A、B、C、D、E、F、G均为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如图所示:
已知A、B、C、D、E、F、G均为常见的物质,其中B、E、G属于单质,反应②是炼铁工业中的主要反应,它们之间的相互转化关系如图所示:
 如图是初中化学实验的几种常用仪器,请按要求填空.
如图是初中化学实验的几种常用仪器,请按要求填空.