题目内容
实验室有以下两种途径制取铜: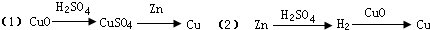
假设每步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法中正确的是( )
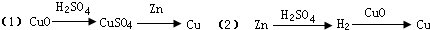
假设每步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法中正确的是( )
| A、消耗等质量的H2SO4 |
| B、消耗等质量的CuO |
| C、生成等质量的ZnSO4 |
| D、所有反应的类型都相同 |
考点:物质的相互转化和制备,反应类型的判定
专题:物质的制备
分析:根据化学方程式的意义,由两种途径的反应方程式及制取过程中的注意事项,根据要制得等质量的铜,分析有关量的关系;根据反应物、生成物的种类既反应的特点分析反应的类型.
解答:解:(1)第一种方案:CuO+H2SO4=CuSO4+H2O,CuSO4+Zn=ZnSO4+Cu.说明生成64克铜需要65克锌和160克硫酸铜,同时生成硫酸锌的质量为161克;生成160克硫酸铜需要80克氧化铜和98克硫酸,反应的类型有复分解反应和置换反应;
(2)第二种方案:Zn+H2SO4=ZnSO4+H2↑,H2+CuO
Cu+H2O.根据氢气还原氧化铜的实验注意事项可知,氢气要通入一段时间后才开始加热反应,因此氢气是过量的.所以生成64克铜需要氧化铜的质量等于80克,需要氢气的质量大于2克;生成大于2克的氢气需要锌的质量大于65克,需要硫酸的质量大于98克,同时生成硫酸锌的质量大于161克;反应的类型只有置换反应.综合上述分析可知:
A、消耗H2SO4的质量不相等.故A错误;
B、消耗等质量的CuO.故B正确;
C、生成ZnSO4的质量不相等.故C错误;
D、所有反应的类型不同.故D错误.
故选B.
(2)第二种方案:Zn+H2SO4=ZnSO4+H2↑,H2+CuO
| ||
A、消耗H2SO4的质量不相等.故A错误;
B、消耗等质量的CuO.故B正确;
C、生成ZnSO4的质量不相等.故C错误;
D、所有反应的类型不同.故D错误.
故选B.
点评:解答本题的关键是掌握氢气还原氧化铜实验的操作方法,即氢气是过量的,所以需要硫酸和锌的质量也过量的.

练习册系列答案
相关题目
使CaCO3与浓盐酸反应,分别用等质量、等容积的集气瓶在相同的温度和压强下按以下不同方法收集上述反应产生的气体各一瓶:
①使产生的气体通过饱和NaHCO3溶液后再收集
②使产生的气体通过饱和NaHCO3溶液和浓H2SO4后再收集
③直接收集
称量三瓶气体的结果是( )
①使产生的气体通过饱和NaHCO3溶液后再收集
②使产生的气体通过饱和NaHCO3溶液和浓H2SO4后再收集
③直接收集
称量三瓶气体的结果是( )
| A、①最重 | B、②最重 |
| C、③最重 | D、三瓶气体一样重 |
在一定条件下,下列物质间的转化不能一步实现的是( )
| A、CO2→O2 |
| B、S→SO3 |
| C、CuSO4→Cu |
| D、Na2CO3→NaOH |
金刚石、石墨都是由同一种元素组成的单质,化学上把这种现象称为这种元素的同素异形体.下列不属于同素异形体的是( )
| A、石墨与“足球烯”(C60) |
| B、红磷(P)与白磷(P4) |
| C、氧气与臭氧(O3) |
| D、生铁与钢 |
 某同学用如图的形式对所学知识进行归纳,其中甲包含了乙、丙、丁….下表是他对四类物质的具体归类,请你填写丁中的内容:
某同学用如图的形式对所学知识进行归纳,其中甲包含了乙、丙、丁….下表是他对四类物质的具体归类,请你填写丁中的内容: