题目内容
使CaCO3与浓盐酸反应,分别用等质量、等容积的集气瓶在相同的温度和压强下按以下不同方法收集上述反应产生的气体各一瓶:
①使产生的气体通过饱和NaHCO3溶液后再收集
②使产生的气体通过饱和NaHCO3溶液和浓H2SO4后再收集
③直接收集
称量三瓶气体的结果是( )
①使产生的气体通过饱和NaHCO3溶液后再收集
②使产生的气体通过饱和NaHCO3溶液和浓H2SO4后再收集
③直接收集
称量三瓶气体的结果是( )
| A、①最重 | B、②最重 |
| C、③最重 | D、三瓶气体一样重 |
考点:气体的净化(除杂)
专题:结合课本知识的信息
分析:根据浓盐酸的挥发性和盐酸能与碳酸氢钠溶液反应生成二氧化碳分析,同时考虑浓硫酸的吸水性.
解答:解:浓盐酸与碳酸钙反应后,得到气体为CO2、H2O蒸气、HCl气体;
通过①收集发生反应NaHCO3+HCl=NaCl+H2O+CO2↑剩余气体为CO2、H2O;
通过②收集发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,但气体由于通过浓硫酸水蒸气被吸收,剩余气体为CO2
通过③包括原始气体CO2、H2O、HCl
通过计算可知道36.5克的HCl可生成44克CO2,且带出部分水蒸气,因此经过碳酸氢钠溶液后气体质量增加,而②因通过浓硫酸水蒸气被吸收,所以①最重;
故选A
通过①收集发生反应NaHCO3+HCl=NaCl+H2O+CO2↑剩余气体为CO2、H2O;
通过②收集发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,但气体由于通过浓硫酸水蒸气被吸收,剩余气体为CO2
通过③包括原始气体CO2、H2O、HCl
通过计算可知道36.5克的HCl可生成44克CO2,且带出部分水蒸气,因此经过碳酸氢钠溶液后气体质量增加,而②因通过浓硫酸水蒸气被吸收,所以①最重;
故选A
点评:此题不但要考虑产生的气体的成分,还要考虑通过不同溶液后气体质量的变化.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质由分子构成的是( )
| A、金刚石 | B、氯化钠 |
| C、蒸馏水 | D、锌 |
能检验和除去酒精中含有的少量水的物质是( )
| A、CuSO4 |
| B、Ca(OH)2 |
| C、CaCO3 |
| D、CaO |
下列说法正确的是( )
| A、氧离子的电子数少于氧原子的电子数 |
| B、氢氧化钠能去除油污,可直接用做厨房的清洁剂 |
| C、把100 g12%的氯化钠溶液配制成6%的氯化钠溶液,需加水100 g |
| D、100 g9.8%硫酸溶液与100 g20.8%的氯化钡溶液反应,所得溶液质量为200 g |
下列物质之间的转化能够通过一步反应实现的是( )
| A、Cu→CuSO4 |
| B、BaSO4→H2SO4 |
| C、NaNO3→NaOH |
| D、CaCl2→CaCO3 |
实验室有以下两种途径制取铜: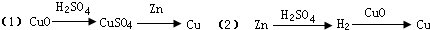
假设每步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法中正确的是( )
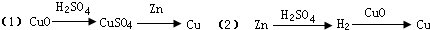
假设每步反应都完全,要制得等质量的铜,两个途径相比较,下列有关说法中正确的是( )
| A、消耗等质量的H2SO4 |
| B、消耗等质量的CuO |
| C、生成等质量的ZnSO4 |
| D、所有反应的类型都相同 |
1991年著名化学家张青莲教授与另外一位化学家合作,测定了铟元素的相对原子量的最新值.铟元素的核电荷数为49,相对原子量为115,铟元素的核外电子数为( )
| A、49 | B、115 |
| C、66 | D、无法确定 |