题目内容
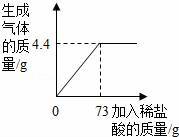
下列四个图象分别对应四种操作过程,其中不正确的是( )
A.

向NaOH溶液中滴加HCl至过量
B.

向CaCl2溶液中通入CO2气体
C.

向CuCl2和HCl的混合溶液中加入过量NaOH溶液
D.

向两份同体积和同质量分数的HCl溶液中分别加入足量的铁粉和镁粉
【考点】酸的化学性质;二氧化碳的化学性质;金属活动性顺序及其应用.
【专题】压轴实验题;图表分析,寻找有效数据.
【分析】A、主要分析反应NaOH+HCl=NaCl+H2O反应前后溶液PH的变化;
B、主要分析向CaCl2溶液中通入CO2后,生成沉淀的变化;
C、主要是要考虑加入NaOH溶液首先是和盐酸发生反应,没有沉淀产生,继续加NaOH溶液才和CuCl2反应,生成沉淀;
D、由于Mg比Fe活泼,所以二者和盐酸反应速度不一样,Mg反应要快.
【解答】解:A、发生的反应为NaOH+HCl=NaCl+H2O,起点是溶液PH大于7,正好反应时为溶液,PH为7,盐酸过量是PH小于7,所以A图象正确;
B、CaCl2溶液和CO2不会发生反应,不能生成沉淀,所以B图象错误;
C、加入NaOH溶液首先发生反应NaOH+HCl=NaCl+H2O,没有沉淀产生,继续加NaOH溶液发生反应CuCl2+2NaOH=Cu(OH)2↓+2NaCl,生成Cu(OH)2沉淀,当NaOH过量时不溶解,所以C图象正确;
D、发生的反应为Fe+2HCl=FeCl2+H2↑,Mg+2HCl=MgCl2+H2↑,因为加入的盐酸质量相等,Mg和Fe足量,根据化学方程式可知生成的H2质量相等,但由于Mg比Fe活泼,所有Mg和盐酸首先反应完,所用时间少,所以D图象正确.
根据题意要求选不正确的,所以选B.
故选B
【点评】首先判断一个图象的正误要抓住三个点(起点、转折点、终点),一个意义(图象的纵横坐标表示的意义);
其次要对图象涉及的化学反应原理(最好用化学方程式表示出来)认真分析;
最后结合以上两点逐一排除、对比可准确作答.

 名校课堂系列答案
名校课堂系列答案某化学兴趣小组对“NaOH溶液与稀盐酸是否恰好完全反应”进 行探究。请你参与他们的探究活动,并回答有关问题。
行探究。请你参与他们的探究活动,并回答有关问题。
【实验探究】
(1)方案一:某同学按右图所示的方法先向试管中加入约2mL NaOH溶液,再滴入几滴酚酞溶液,溶液变红。然后慢慢滴入稀盐酸,边滴边振荡,直至溶液
恰好变为 色, 证明NaOH溶液与稀盐酸恰好完全反应。
证明NaOH溶液与稀盐酸恰好完全反应。
①请指出右图操作中的错误 。
②写出NaOH溶液与稀盐酸反应的化学方程式 。
(2 )方案二:
)方案二:
| 实验步骤 | 实验现象 | 结论 |
| 取2m | 若 | 稀盐酸过量 |
| 若没有明显现象 | NaOH溶液与稀盐酸恰好完全反应 |
【实验反思】
(3) 方案一在滴入稀盐酸的过程中,若观察到曾有少量气泡出现, 请分析产生气泡的原因可能是 (写出一条即可)。
(4)有同学提出方案二不能证明NaOH溶液与稀盐酸恰好完全反应,其原因是 。为此,还需要选择  (填一种试剂),再进行实验即可。
(填一种试剂),再进行实验即可。
【拓展应用】
(5)请举一例说明中和反应在生产生活中的应用 。


 L NaOH溶液于试管中中,滴入一定量的稀盐酸,振振荡后加入镁条
L NaOH溶液于试管中中,滴入一定量的稀盐酸,振振荡后加入镁条


 CO2↑+CO↑+H2O.某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁.请根据题目要求回答下列问题:
CO2↑+CO↑+H2O.某化学兴趣小组同学设计如下实验装置,用于制取纯净干燥的CO气体来还原氧化铁.请根据题目要求回答下列问题: