题目内容
4. 某化学小组同学为了测定实验室一瓶稀盐酸中溶质的质量分数.
某化学小组同学为了测定实验室一瓶稀盐酸中溶质的质量分数.他们用铜锌合金和此稀盐酸完成了如图的实验.
(1)恰好完全反应时生成氢气的质量是0.2g;
(2)该瓶稀盐酸中溶质的廣量分数.
分析 依据铜锌合金中锌能够和盐酸反应时只有锌能反应而铜不反应,利用质量守恒定律可以求出氢气的质量,利用氢气的质量,根据反应的化学方程式求出参加反应的氯化氢质量,据此分析解答;
解答 解:
(1)依据反应中锌和盐酸反应可以生成氢气,根据质量守恒定律,生成氢气的质量为10g+100g-109.8g=0.2g
(2)设参加反应的氯化氢质量为x.
Zn+2HCl═ZnCl2+H2↑
73 2
x 0.2g
$\frac{73}{x}=\frac{2}{0.2g}$
x=7.3g
该瓶盐酸溶液溶质质量分数为$\frac{7.3g}{100g}$×100%=7.3%
故答案为:
(1)0.2;
(2)该瓶盐酸溶液溶质质量分数为7.3%
点评 本题主要考查学生根据化学方程式进行计算的能力,明确生成氢气的质量和对应的化学反应的关系是解答本题的关键.

练习册系列答案
相关题目
14.化学兴趣小组提纯粗盐,再用制得的精盐配制一定溶质质量分数的氯化钠溶液,下列说法正确的是( )
| A. | 过滤粗盐水时,用玻璃棒搅拌以加快过滤 | |
| B. | 蒸发滤液时,待蒸发皿中滤液蒸干后才停止加热 | |
| C. | 配制溶液时要经过计算、称量和量取、溶解、装瓶等步骤 | |
| D. | 配制溶液需要的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等 |
15.根据表中NaCl和KNO3溶解度数据,回答下列问题.
①40℃时,NaCl的溶解度是36.6g.
②20℃时,将等质量KNO3和NaCl固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到60℃时现象如图2(不考虑水分蒸发).
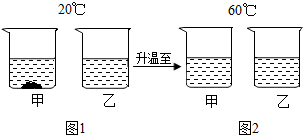
根据图1和图2现象判断:甲烧杯中的固体是KNO3;将图2中的两溶液降温至40℃时,对两种溶液的分析正确的是BC.
A.甲一定是饱和溶液 B.两溶液中溶质质量分数一定相等 C.乙一定是不饱和溶液
D.甲一定会析出晶体 E.甲溶液浓度一定大于乙溶液浓度
③如果60℃时KNO3饱和溶液中混有少量NaCl时,提纯KNO3可采用方法降温结晶.
④将等质量KNO3的饱和溶液和NaCl的饱和溶液从60℃降温到20℃后,所得溶液中溶质质量分数大的是NaCl 溶液.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| NaCl溶解度(g/100g水) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3溶解度(g/100g水) | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
②20℃时,将等质量KNO3和NaCl固体,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到60℃时现象如图2(不考虑水分蒸发).

根据图1和图2现象判断:甲烧杯中的固体是KNO3;将图2中的两溶液降温至40℃时,对两种溶液的分析正确的是BC.
A.甲一定是饱和溶液 B.两溶液中溶质质量分数一定相等 C.乙一定是不饱和溶液
D.甲一定会析出晶体 E.甲溶液浓度一定大于乙溶液浓度
③如果60℃时KNO3饱和溶液中混有少量NaCl时,提纯KNO3可采用方法降温结晶.
④将等质量KNO3的饱和溶液和NaCl的饱和溶液从60℃降温到20℃后,所得溶液中溶质质量分数大的是NaCl 溶液.
19.2015年4月6日,福建漳州古雷PX工厂腾龙芳烃乙库凝析油外抽室发生爆炸,方圓百里震感强烈.事发后,消防及相关部门赶赴现场进行救援,下列措施与灭火原理无关的是( )
| A. | 采取喷水降温 | |
| B. | 携带侦毒器、侦毒管、辐射仪等侦毒设备 | |
| C. | 用灭火毯盖紧油罐和卸油口 | |
| D. | 关闭如油机,用水路隔离 |
9.在Mg(NO3)2和AgNO3的混合溶液中,加入过量的锌粉,充分反应后过滤.据此得出的结论不正确的是( )
| A. | 滤渣中一定有Zn和Ag | B. | 滤渣中一定有Mg和Ag | ||
| C. | 滤液中一定有Zn(NO3)2 | D. | 滤液中一定有Mg(NO3)2 |
13.“低碳生活”代表着更健康、更自然、更安全的生活,同时也是一种低成本,低代价的生活方式,下列做法不符合低碳生活的是( )
| A. | 用淘米水浇花 | |
| B. | 少用纸巾,重拾手帕,保护森林 | |
| C. | 步行或骑自行车上学 | |
| D. | 提倡使用一次性用品,如一次性木筷等 |
14.正确的实验操作对实验结果,人身安全都非常重要.下列实验操作正确的( )
| A. | 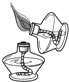 点燃酒精灯 | B. | 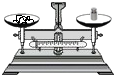 称量10.05g固体 | C. |  液体加热 | D. |  量9.5mL液体 |
 .(在答题纸上画图表示并作简要说明)
.(在答题纸上画图表示并作简要说明)