题目内容
20.如图(甲)所示,A,B,C,D初中化学中常见的单质,甲、乙分别是甲烷燃烧时生成的两种物质,丁是常用建筑材料的主要成分,G为无色有刺激性气味的气体,能使紫色石蕊变蓝,J是赤铁矿的主要成分.
(1)写出下列物质的化学式:丙:H2CO3;G:NH3;
(2)写出下列化学方程式:
①丁高温分解:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;②H与J反应:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)如图(乙)所示,向装有水的小试管中加物质E后,U型管中两边的红墨水液面变化情况是A.
A.左低右高 B.左高右低 C.与原来一样
(4)在上题中除了加入物质E外,还有哪些物质也会产生相同现象氢氧化钠(写一种物质名称即可).
分析 根据A、B、C、D初中化学中常见的单质,J是赤铁矿的主要成分,所以J是氧化铁,G为无色有刺激性气味的气体,能使紫色石蕊变蓝,所以G是氨气,丁是常用建筑材料的主要成分,碳酸钙高温分解会生成氧化钙和二氧化碳,E和甲会生成碱F,所以E是氧化钙,乙是二氧化碳,氧化钙和水会生成氢氧化钙,所以甲是水,F是氢氧化钙,二氧化碳和C反应生成的H会与氧化铁反应生成D,所以H是一氧化碳,C是碳,一氧化碳和氧化铁高温生成铁和二氧化碳,所以D是铁,碳和B点燃会生成二氧化碳,所以B是氧气,A和氧气反应会生成水,所以A是氢气,水和二氧化碳反应生成碳酸,所以丙是碳酸,碳酸和氢氧化钙反应生成碳酸钙和水,然后将推出的物质进行验证即可.
解答 解:(1)A、B、C、D初中化学中常见的单质,J是赤铁矿的主要成分,所以J是氧化铁,G为无色有刺激性气味的气体,能使紫色石蕊变蓝,所以G是氨气,丁是常用建筑材料的主要成分,碳酸钙高温分解会生成氧化钙和二氧化碳,E和甲会生成碱F,所以E是氧化钙,乙是二氧化碳,氧化钙和水会生成氢氧化钙,所以甲是水,F是氢氧化钙,二氧化碳和C反应生成的H会与氧化铁反应生成D,所以H是一氧化碳,C是碳,一氧化碳和氧化铁高温生成铁和二氧化碳,所以D是铁,碳和B点燃会生成二氧化碳,所以B是氧气,A和氧气反应会生成水,所以A是氢气,水和二氧化碳反应生成碳酸,所以丙是碳酸,碳酸和氢氧化钙反应生成碳酸钙和水,经过验证,推导正确,所以丙是H2CO3,G是NH3;
(2)丁高温分解的反应是碳酸钙在高温的条件下反应生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
H与J反应的反应是一氧化碳和氧化铁在高温的条件下反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)向装有水的小试管中加物质氧化钙后,氧化钙和水反应生成氢氧化钙,放出热量,U型管中两边的红墨水液面左低右高,故选:A;
(4)通过分析可知,除了氧化钙还有氢氧化钠.
故答案为:(1)H2CO3,G是NH3;
(2)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)A;
(4)氢氧化钠.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

(1)日常生活中使用的牙膏里面都含有一定量的摩擦剂,根据你的生活经验推测,摩擦剂应具备下列性质中的BC(填字母);
A.易溶于水 B.难溶于水 C.坚硬 D.柔软
(2)牙膏摩擦剂碳酸钙可以用石灰石来制取.张华同学设计了一种制备碳酸钙的实验方案,其流程如下(第③个反应原理Na2CO3+Ca(OH)2═CaCO3↓+2NaOH):

请写出上述方案中第②步有关反应的化学方程式:CaO+H2O═Ca(OH)2;
李方同学仍用石灰石为原料,设计了另一种制备碳酸钙的实验方案,流程如下:
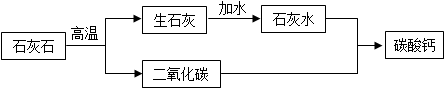
李方认为自己设计的方案比张华更好,其优点是减少二氧化碳的排放,产物充分利用.
(3)珍珠是一种名贵的中药材,它含有碳酸钙、蛋白质、十几种氨基酸和多种微量元素.某兴趣小组利用已学过的化学知识,按下图所示的实验过程,来测定本地某品牌珍珠粉中碳酸钙的质量分数,并分成甲、乙两个小组分别进行对照实验测定.
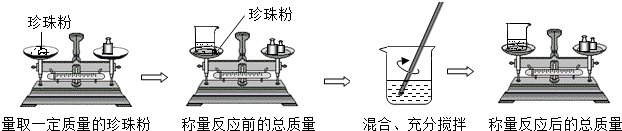
①兴趣小组将密度为1.18g/mL,37%的浓盐酸配制成20%的185g的稀盐酸,用于实验.
配制的步骤有计算、量取、稀释;使用的玻璃仪器有量筒、烧杯、玻璃棒和胶头滴管,计算所得需要水的体积为85mL.
②两个小组测量数据记录如下(只考虑碳酸钙与盐酸反应,杂质不与酸反应且盐酸足量):
| 组别 | 珍珠粉的质量/g | 反应前的总质量/g | 反应后的总质量/g |
| 甲 | 1.25 | 151.25 | 150.81 |
| 乙 | 12.5 | 162.5 | 158.1 |
根据正确的数据,请你计算出珍珠粉中碳酸钙的质量分数为80%.
Ⅰ.根据下列实验室制备气体的有关装置图回答有关问题:
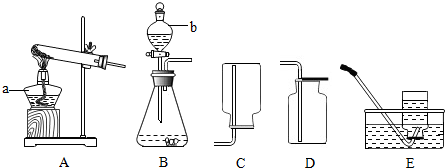
(1)写出仪器a、b的名称.a是酒精灯;b是分液漏斗.
(2)若用A装置制取氧气,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.制取甲烷的发生装置应选择A(填编号,下同),收集较纯净甲烷应选E;请写出甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
Ⅱ.松花蛋,又称皮蛋是餐桌一美味.加工松花蛋的一种工艺的主要原料为:鸭蛋、水、生石灰、纯碱、食盐.加工时,将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.
请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应放出大量热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色.
(4)同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中含有哪些溶质?
【作出假设】①甲同学推断:NaOH、NaCl
②乙同学推断:NaOH、NaCl、Na2CO3
③丙同学推断:NaOH、NaCl、Ca(OH)2
④丁同学推断:NaOH、NaCl、Ca(OH)2、Na2CO3
通过进一步讨论,大家一致认为丁同学的推断是错误的,理由是(用化学方程式表示)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量上层料液,滴加稀盐酸 | 无明显现象 | 丙同学的推断是正确的. |
| 另取少量上层料液,滴加碳酸钠溶液 | 生成白色沉淀 |
| A. | 塑料餐具 | B. | 木质菜板 | C. | 陶瓷碗 | D. | 不锈钢菜刀 |
| A. | 一氧化碳、二氧化碳 | B. | 二氧化碳、碳酸 | ||
| C. | 二氧化碳、氢氧化钙 | D. | 二氧化碳、碳酸钙 |
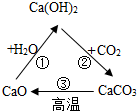 完成下列反应的化学方程式,并回答有关问题,请你用化学方程式表示如图中的三个化学反应
完成下列反应的化学方程式,并回答有关问题,请你用化学方程式表示如图中的三个化学反应 A、B、C、D、E为五种不同类别的纯净物,他们之间的反应关系如图.“”表示两种物质之间能相互转化,“-”表示两物质之间能发生化学反应.其中,A为金属单质,B为赤铁矿的主要成分,E的水溶液为黄色.请回答:
A、B、C、D、E为五种不同类别的纯净物,他们之间的反应关系如图.“”表示两种物质之间能相互转化,“-”表示两物质之间能发生化学反应.其中,A为金属单质,B为赤铁矿的主要成分,E的水溶液为黄色.请回答: