题目内容
6. 实验室有一瓶未开封的浓盐酸,标签部分内容如图所示
实验室有一瓶未开封的浓盐酸,标签部分内容如图所示(1)若取出浓盐酸50mL,加水100mL,得到的稀盐酸的溶质质量分数是多少?
(2)若用这瓶浓盐酸来配制200g溶质质量分数为10%的稀盐酸,需浓盐酸和水各多少毫升?(水的密度是1.0g/cm3)
分析 (1)根据溶质的质量分数公式分析.
(2)根据溶液稀释前后溶液中溶质的质量不变,便可轻松求解.
解答 解:(1)浓盐酸50mL的质量为50mL×1.18g/mL=59g,水100mL的质量为•100mL×1.0g/mL=100g,
得到的稀盐酸的溶质质量分数是$\frac{59g×37%}{59g+100g}×100%$=13.7%
(2)设:需量取浓盐酸的质量为m.
200g×10%=m•37%
m≈54.1g
根据密度公式:ρ=$\frac{m}{v}$,所以需量取浓盐酸的体积V=54.1g÷1.18g/cm3≈45.8mL
需要水的质量为:200克-54.1克=145.9克 即145.9mL
故答案为:(1)13.7%,(2)45.8,145.9.
点评 该题充分的体现了用化学的知识去解决生活中的问题,要求学生要熟练的掌握有关溶液中溶质质量分数的计算问题;进行有关溶液计算时溶液质量等于溶剂质量和溶质质量之和,但是溶液体积不等于溶剂体积和溶质体积之和.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
16.下列对生产、生活现象的解释正确的是( )
| A. | 在花园里可嗅到花香,因为分子在不断运动 | |
| B. | 铝锭难被压缩,因为铝原子间没有间隙 | |
| C. | 石油气加压后贮存在钢瓶中,因为气体分子体积很小 | |
| D. | 温度计里的汞柱下降,因为原子随温度的降低而变小 |
17.下列实验基本操作错误的是( )
| A. | 制取气体时应先检查装置的气密性 | |
| B. | 给试管里液体加热,液体应不超过试管容积的1/3 | |
| C. | 给试管加热时,应用手拿住试管夹的短柄 | |
| D. | 取用固体药品,一般用药匙,有些块状药品可用镊子夹取 |
18.对物质的性质进行比较归纳,有利于更好的学习科学,下列对物质性质的归纳中,正确的是( )
| A. | H2、O2、CH4都具有可燃性 | |
| B. | 浓硫酸、浓盐酸、酒精都具有挥发性 | |
| C. | H2、C、CO都能和CuO发生置换反应 | |
| D. | Fe、Al、Cu都能和AgNO3溶液发生置换反应 |
15.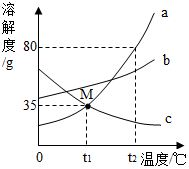 如图是不含结晶水的a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是不含结晶水的a、b、c三种物质的溶解度曲线,下列说法正确的是( )
 如图是不含结晶水的a、b、c三种物质的溶解度曲线,下列说法正确的是( )
如图是不含结晶水的a、b、c三种物质的溶解度曲线,下列说法正确的是( )| A. | t2℃时,将50ga物质加入到50g水中充分搅拌,得到100ga的饱和溶液 | |
| B. | 用等质量的a、b、c三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液>b溶液>a溶液 | |
| C. | 将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液M中溶质的质量分数的大小关系是:b>a=c | |
| D. | 将t2℃时,a、b两种物质的饱和溶液降温到t1℃时,析出晶体的质量:a>b |
16.下列物之间的转化,能通过一步反应实验的是( )
①C2H5OH→CO2②CaO→Ca(OH)2③H2O2→H2O④Cu→CuCl2⑤Fe3O4→Fe.
①C2H5OH→CO2②CaO→Ca(OH)2③H2O2→H2O④Cu→CuCl2⑤Fe3O4→Fe.
| A. | ①②③④ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
 等质量的两种常见金属A和B(状态相同或者状态颗粒大小对反应影响忽略不计),分别与足量的稀硫酸反应,生成正二价的金属硫酸盐和氢气.生成氢气的质量与时间关系如图,请结合所学知识回答:
等质量的两种常见金属A和B(状态相同或者状态颗粒大小对反应影响忽略不计),分别与足量的稀硫酸反应,生成正二价的金属硫酸盐和氢气.生成氢气的质量与时间关系如图,请结合所学知识回答: