题目内容
3.下列情况①煤的燃烧②工业废气的任意排放③人工呼吸④飞机汽车尾气的排放,可引起大气污染的是( )| A. | ①②③ | B. | ③④ | C. | ①②③④ | D. | ①②④ |
分析 随着现代化工业的发展,排放到空气中的有害物质改变了空气的成分,造成对空气的污染,造成对空气污染的有害物质大致可分为:粉尘和气体两大类.从世界范围看,排放到空气中的有害气体主要有二氧化硫,一氧化碳,二氧化氮.
解答 解:①煤的燃烧②工业废气的任意排放④飞机汽车尾气的排放等都会产生大量的有害气体和粉尘,引起大气污染.③人工呼吸,产生二氧化碳,二氧化碳不属于大气污染物,不会引起大气污染.
故选D.
点评 了解典型的大气环境问题与排放到大气中的物质的联系是解答此题的关键.关于CO2,它不属于大气污染物,但是CO2排放过量的话会引起“温室效应”,请学生们注意.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13. 常温下,H2O2分解生成O2的速率较为缓慢.研究性学习小组选择“H2O2 分解生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
常温下,H2O2分解生成O2的速率较为缓慢.研究性学习小组选择“H2O2 分解生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】催化剂的种类会影响H2O2 分解生成O2的快慢.
【实验方案】常温下,取两份同体积,同浓度H2O2的溶液,分别加入二氧化锰和氯化钠固体,测量各生成一瓶相同体积的O2所需的时间.
【实验装置】如图是他们进行实验的装置图
【实验操作】检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.实验记录如表:
【结论】该探究过程得出的结论是在相同条件下,H2O2生成O2的快慢与催化剂种类有关.
【反思】若要证明二氧化锰、氯化钠固体是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
【交流讨论】小华同学提出,H2O2分解生成O2的快 慢还与哪些因素有关?请你帮助他们继续探究.(提出一种影响H2O2分解生成O2快慢的因素以及相关假设,并设计实验方案)
【你的假设】H2O2生成氧气的快慢与过氧化氢的浓度有关
【设计方案】
实验方法及步骤可能观察到的实验现象实验结论假设正确.
 常温下,H2O2分解生成O2的速率较为缓慢.研究性学习小组选择“H2O2 分解生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
常温下,H2O2分解生成O2的速率较为缓慢.研究性学习小组选择“H2O2 分解生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:【假设】催化剂的种类会影响H2O2 分解生成O2的快慢.
【实验方案】常温下,取两份同体积,同浓度H2O2的溶液,分别加入二氧化锰和氯化钠固体,测量各生成一瓶相同体积的O2所需的时间.
【实验装置】如图是他们进行实验的装置图
【实验操作】检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶放出的气体.实验记录如表:
| 实验编号 | ① | ② |
| 反应物 | 5%H2O2 100mL | 5%H2O2 100mL |
| 加入固体 | 氯化钠固体 | 0.5g二氧化锰 |
| 收集气体所需时间 | 165s | 46s |
【反思】若要证明二氧化锰、氯化钠固体是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的质量和化学性质是否改变.
【交流讨论】小华同学提出,H2O2分解生成O2的快 慢还与哪些因素有关?请你帮助他们继续探究.(提出一种影响H2O2分解生成O2快慢的因素以及相关假设,并设计实验方案)
【你的假设】H2O2生成氧气的快慢与过氧化氢的浓度有关
【设计方案】
实验方法及步骤可能观察到的实验现象实验结论假设正确.
14.下列变化属于化学变化的是( )
| A. | 烧开水 | B. | 电解水 | C. | 水结冰 | D. | 蔗糖溶于水 |
11.元素间的本质区别是( )
| A. | 相对原子质量 | B. | 最外层电子数 | C. | 中子数 | D. | 质子数 |
18.比较、推理是化学学习常用的方法.以下是根据一些反应事实推导出的影响化学反应的因素,其中不合理的是( )
| 化学反应事实 | 影响反应的因素 | |
| A | 铁丝在空气中很难燃烧,在氧气中能剧烈燃烧 | 反应物的浓度 |
| B | 碳在常温下不与氧气反应,在点燃时能与氧气反应 | 反应的温度 |
| C | 过氧化氢在常温下较难分解,在加入二氧化锰后迅速分解 | 催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
| A. | A | B. | B | C. | C | D. | D |
8.下列有关实验现象的描述正确的是( )
| A. | 铁丝在氧气中燃烧时火星四射,有黑色四氧化三铁固体生成 | |
| B. | 铁与稀盐酸反应有气泡产生,溶液由无色变成了浅绿色 | |
| C. | 红磷在空气中燃烧产生大量白色烟雾 | |
| D. | 将黄铜与纯铜互相刻划,黄铜表面出现划痕 |
12.某工化肥厂需大量二氧化碳生产化肥,欲购进一批石灰石(其中杂质不参加任何反应),厂家到产地取样分析以确定价格.他们取样2克,并把20克稀盐酸分四次加入,充分反应后,每次剩余固体质量见表
试计算:
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
| 稀盐酸的用量 | 剩余固体的质量/g |
| 第一次加入5g | 1.4g |
| 第二次再加入5g | 0.8g |
| 第三次再加入5g | 0.4g |
| 第四次再加入5g | 0.4g |
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
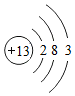 (1)用正确的化学用语填空:
(1)用正确的化学用语填空: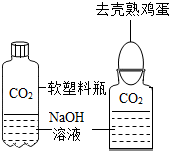 该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?
该兴趣小组同学将制得的CO2分别通人澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象.CO2和NaOH是否发生了化学反应?