题目内容
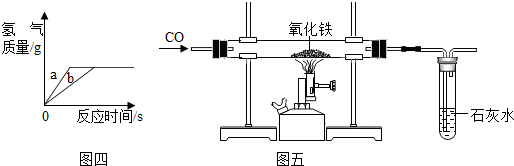
根据所学知识并结合图所示装置回答下列问题.
(1)图中标有①、②的仪器名称:① ; ② .
(2)实验室用高锰酸钾制取氧气,可选用 (填标号)装置和D装置的组合,发生反应的化学方程式为 .
(3)实验室用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为 ;实验后可回收重复使用的药品是 .
(4)实验室欲制取并收集一定量的二氧化碳气体,应选用的装置是 ; 发生反应的化学方程
式为 .如何验证CO2已收集满? .
(5)验证CO2方法是:在澄清的石灰水中通入二氧化碳,现象是 ,发生反应的化学方程式为 .
(6)硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04.
①在图中,应选用图 作为制取H2S的装置.
②收集H2S气体时,应从图F装置中的 (填“a”或“b”)导管进入,对产生尾气的处理方法是: .

(1)图中标有①、②的仪器名称:①
(2)实验室用高锰酸钾制取氧气,可选用
(3)实验室用过氧化氢溶液与二氧化锰制取氧气,反应的化学方程式为
(4)实验室欲制取并收集一定量的二氧化碳气体,应选用的装置是
式为
(5)验证CO2方法是:在澄清的石灰水中通入二氧化碳,现象是
(6)硫化氢(H2S)是一种具有臭鸡蛋气味的致命毒气,它的密度比空大,可溶于水形成氢硫酸,氢硫酸具有酸的通性.实验室常用固体硫化亚铁(FeS)和稀硫酸在常温下制得H2S,同时生成FeS04.
①在图中,应选用图
②收集H2S气体时,应从图F装置中的
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的检验和验满,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)据常用仪器回答;
(2)实验室用高锰酸钾制取氧气,属于固体加热型,故选发生装置A,并据反应原理书写方程式;
(3)据过氧化氢溶液分解的反应原理书写方程式,二氧化锰的质量和化学性质在反应前后不变,所以可重复使用;
(4)实验室制取二氧化碳用大理石和稀盐酸反应,不需加热,属于固液常温型,故选发生装置B,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,据反应原理书写方程式;验满二氧化碳的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(5)二氧化碳能使澄清的石灰水变浑浊,据反应原理书写方程式;
(6)①根据反应物的状态、反应条件可以选择发生装置;
②根据气体的密度和溶解性选择收集方法,硫化氢气体溶于水形成氢硫酸,氢硫酸具有酸的通性,可与碱性溶液反应.
(2)实验室用高锰酸钾制取氧气,属于固体加热型,故选发生装置A,并据反应原理书写方程式;
(3)据过氧化氢溶液分解的反应原理书写方程式,二氧化锰的质量和化学性质在反应前后不变,所以可重复使用;
(4)实验室制取二氧化碳用大理石和稀盐酸反应,不需加热,属于固液常温型,故选发生装置B,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,据反应原理书写方程式;验满二氧化碳的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(5)二氧化碳能使澄清的石灰水变浑浊,据反应原理书写方程式;
(6)①根据反应物的状态、反应条件可以选择发生装置;
②根据气体的密度和溶解性选择收集方法,硫化氢气体溶于水形成氢硫酸,氢硫酸具有酸的通性,可与碱性溶液反应.
解答:解:(1)标号仪器分别是试管、长颈漏斗;
(2)实验室用高锰酸钾制取氧气,属于固体加热型,故选发生装置A,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是2KMnO4
K2MnO4+MnO2+O2↑;
(3)过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,反应方程式是2H2O2
2H2O+O2↑;二氧化锰的质量和化学性质在反应前后不变,所以可重复使用;
(4)实验室制取二氧化碳用大理石和稀盐酸反应,不需加热,属于固液常温型,故选发生装置B,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;验满二氧化碳的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(5)二氧化碳能使澄清的石灰水变浑浊,所以在澄清的石灰水中通入二氧化碳,澄清的石灰水会变浑浊,反应方程式是Ca(OH)2+CO2=CaCO3↓+H2O;
(6)①硫化亚铁和稀硫酸反应不需要加热,应该用B装置作为发生装置.
②硫化氢能够溶于水,不能用排水法收集,硫化氢的密度比空气大,可以用向上排空气法收集,用C装置收集硫化氢时,应从C装置中的a导管进入;
因为硫化氢溶于水形成氢硫酸,氢硫酸具有酸的通性,可以用碱性溶液吸收硫化氢,例如可以用氢氧化钠溶液、氢氧化钾溶液等吸收;
故答案为:(1)试管;长颈漏斗;
(2)A;2KMnO4
K2MnO4+MnO2+O2↑;
(3)2H2O2
2H2O+O2↑;二氧化锰;
(4)BC;CaCO3+2HCl═CaCl2+H2O+CO2↑;将燃着的木条放于集气瓶口,若木条熄灭则满;
(5)澄清的石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O;
(6)①A;②a;用氢氧化钠溶液吸收.
(2)实验室用高锰酸钾制取氧气,属于固体加热型,故选发生装置A,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是2KMnO4
| ||
(3)过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,反应方程式是2H2O2
| ||
(4)实验室制取二氧化碳用大理石和稀盐酸反应,不需加热,属于固液常温型,故选发生装置B,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集,方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;验满二氧化碳的方法是将燃着的木条放于集气瓶口,观察木条是否熄灭进行判断;
(5)二氧化碳能使澄清的石灰水变浑浊,所以在澄清的石灰水中通入二氧化碳,澄清的石灰水会变浑浊,反应方程式是Ca(OH)2+CO2=CaCO3↓+H2O;
(6)①硫化亚铁和稀硫酸反应不需要加热,应该用B装置作为发生装置.
②硫化氢能够溶于水,不能用排水法收集,硫化氢的密度比空气大,可以用向上排空气法收集,用C装置收集硫化氢时,应从C装置中的a导管进入;
因为硫化氢溶于水形成氢硫酸,氢硫酸具有酸的通性,可以用碱性溶液吸收硫化氢,例如可以用氢氧化钠溶液、氢氧化钾溶液等吸收;
故答案为:(1)试管;长颈漏斗;
(2)A;2KMnO4
| ||
(3)2H2O2
| ||
(4)BC;CaCO3+2HCl═CaCl2+H2O+CO2↑;将燃着的木条放于集气瓶口,若木条熄灭则满;
(5)澄清的石灰水变浑浊;Ca(OH)2+CO2=CaCO3↓+H2O;
(6)①A;②a;用氢氧化钠溶液吸收.
点评:本题考查知识综合,据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,并掌握实验室制取氧气、二氧化碳的方法、验满、检验方法等进行解答.

练习册系列答案
相关题目
某化合物R 3.2g在氧气中充分燃烧只生成8.8g CO2和7.2g H2O,则R的组成是( )
| A、只含有C、H元素 |
| B、含有C、H、O三种元素 |
| C、一定含有C、H元素,可能含有氧元素 |
| D、无法确定 |
下列实验不能达到预期目的是( )
| A、用肥皂水区别硬水和软水 |
| B、氧气验满用带火星木条伸入集气瓶中 |
| C、可以用排水法收集氧气 |
| D、品尝味道可以区分厨房中的蔗糖和食盐 |