题目内容
19.向Ba(OH)2溶液中逐滴加稀H2SO4至过量,如图可表示溶液导电性实验是( )| A. |  | B. |  | C. |  | D. |  |
分析 根据物质的水溶液能够导电,应能产生自由移动离子;结合氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水,进行分析判断.
解答 解:向Ba(OH)2溶液中逐滴加稀H2SO4至过量,氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水,反应的化学方程式为H2SO4+Ba(OH)2=BaSO4↓+2H2O,随着稀H2SO4的加入,离子浓度逐渐减小,导电性逐渐降低,恰好完全反应时溶液中没有自由移动的离子,即恰好完全反应时导电能力为零;继续滴加稀硫酸,稀硫酸过量,稀硫酸中存在能自由移动的氢离子和硫酸根离子,溶液又能够导电了,溶液中溶液的导电性变化是强→弱(水有微弱的导电性,几乎为0)→强,图象D符合导电性的变化趋势.
故选:D.
点评 本题难度不大,掌握溶液导电的原因(能够产生自由移动的离子)、酸的化学性质并能灵活运用是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.有关分子、原子的说法正确的是( )
| A. | 花香四溢说明分子间有间隔 | |
| B. | 原子是化学变化中的最小粒子 | |
| C. | 气体易被压缩是因为气体分子受压变小 | |
| D. | 化学变化中分子、原子都可分 |
10. 如图是A、B两物质的溶解度曲线,分别得到的下列信息中,正确的是( )
如图是A、B两物质的溶解度曲线,分别得到的下列信息中,正确的是( )
 如图是A、B两物质的溶解度曲线,分别得到的下列信息中,正确的是( )
如图是A、B两物质的溶解度曲线,分别得到的下列信息中,正确的是( )| A. | 溶解度随温度的变化值B大于A | |
| B. | t2℃时,等质量的A、B两饱和溶液降温到t1℃时析出溶质的质量A大于B | |
| C. | t2℃时,B物质的溶解度大于t2℃时A物质的溶解度 | |
| D. | t1℃时,A、B两饱和溶液的溶质质量分数不相等 |
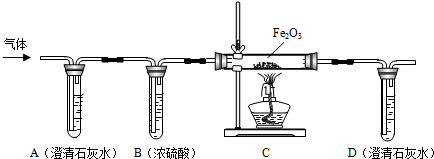
7.在实验探究课上,老师给了同学们一包红色粉未,该粉末是铜粉和氧化铁粉中的一种或两种.同学们为了确定该粉末的成分,进行如下探究,请你参与他们的探究并回答问题.
【猜想】猜想I:红色粉末是铜粉;猜想Ⅱ:红色粉末是氧化铁粉;猜想Ⅲ:红色粉末是铜粉和氧化铁粉的混合物
【实验】经过查阅资料、回忆已学过的知识,
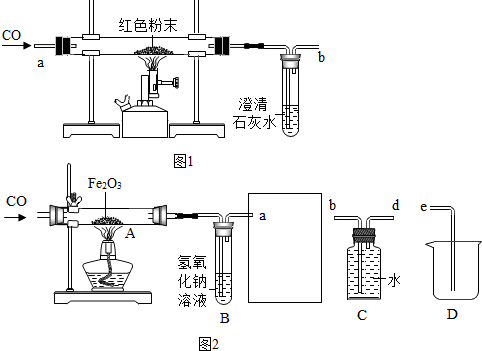
大家决定设计如图1所示的实验进行探究.请完成下列表格:
【表达】通过实验及分析,确定红色粉末是铜粉和氧化铁粉的混合物,则在上述实验过程中所发生反应的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2、-.
【反思】从环保角度看,图1所示的实验装置有不足之处,请说出其中一种改进方法:在b处用酒精灯点燃,或用塑料袋(气球)收集.
【拓展】为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的ABC(填序号).
A.硝酸铜溶液 B.稀盐酸 C.氯化亚铁溶液 D.硫酸镁
【应用】同学们用一氧化碳与氧化铁的反应来模拟炼铁的原理,装置如图2所示,请回答有关问题:
(1)B装置中氢氧化钠溶液的作用是吸收混合气体中的二氧化碳
(2)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→d→b→e.

【猜想】猜想I:红色粉末是铜粉;猜想Ⅱ:红色粉末是氧化铁粉;猜想Ⅲ:红色粉末是铜粉和氧化铁粉的混合物
【实验】经过查阅资料、回忆已学过的知识,
大家决定设计如图1所示的实验进行探究.请完成下列表格:
| 实验中可能出现的现象 | 结论 |
| 红色粉末不变色,石灰水不变浑浊 | 猜想Ⅰ正确 |
| 红色粉末全部变为黑色,石灰水变浑浊 | 猜想Ⅱ正确 |
| 红色粉末部分变为黑色,石灰水变浑浊 | 猜想Ⅲ正确 |
【反思】从环保角度看,图1所示的实验装置有不足之处,请说出其中一种改进方法:在b处用酒精灯点燃,或用塑料袋(气球)收集.
【拓展】为了进一步探究铁和铜的金属活动性强弱,你认为可选用下列试剂中的ABC(填序号).
A.硝酸铜溶液 B.稀盐酸 C.氯化亚铁溶液 D.硫酸镁
【应用】同学们用一氧化碳与氧化铁的反应来模拟炼铁的原理,装置如图2所示,请回答有关问题:
(1)B装置中氢氧化钠溶液的作用是吸收混合气体中的二氧化碳
(2)为避免将CO排放到空气中,并回收利用CO,方框中连接的是C和D装置,导管接口的连接顺序应为a→d→b→e.
4.天然气的主要成分是( )
| A. | 甲烷 | B. | 乙烯 | C. | 一氧化碳 | D. | 氢气 |
11. 某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )
某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )
 某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )
某科学兴趣小组为了测定实验室中久置的NaOH的变质程度,进行了下列实验,先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量,从而进一步确定样品中NaOH的变质程度.实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示.则下列针对本实验的说法中错误的是( )| A. | 产生CO2气体的质量为2.2g | B. | Na2CO3的质量为5.3g | ||
| C. | 变质的NaOH的质量为4.0g | D. | NaOH的变质程度为30% |
9.取一定量的氧化镁与氧化铜的混合物,向其中加入溶质质量分数为14.6%的稀盐酸100g,恰好完全反应生成盐和水.则原混合物中氧元素的质量是( )
| A. | 14.6g | B. | 3.6g | C. | 3.2g | D. | 1.4g |