题目内容
10. 为了加深对质量守恒定律的理解,某校化学实验小组以“镁条在空气中燃烧”实验进行了再探究:
为了加深对质量守恒定律的理解,某校化学实验小组以“镁条在空气中燃烧”实验进行了再探究:(1)镁条在空气中燃烧时观察到的现象是发出耀眼的白光,放出大量的热,生成一种白色固体;
(2)根据质量守恒定律,镁条在空气中燃烧后的质量大于(填“大于”、“等于”或“小于”之一)镁条的质量;原因是生成氧化镁的质量等于参加反应的镁和氧气的质量之和.
(3)化学反应之所以遵循质量守恒定律,从微观上看,是因为反应前后原子的种类、数目、质量均不变.
分析 (1)根据镁条在空气中燃烧时的现象,进行分析解答.
(2)根据质量守恒定律,参加反应的镁和氧气的质量之和等于生成的氧化镁的质量,进行分析解答.
(3)根据微观上遵守质量守恒定律的原因,进行分析解答.
解答 解:(1)镁条在空气中燃烧,发出耀眼的白光,放出大量的热,生成一种白色固体.
(2)由质量守恒定律,参加反应的镁和氧气的质量之和等于生成的氧化镁的质量,镁条在空气中燃烧后的质量大于镁条的质量,原因是生成氧化镁的质量等于参加反应的镁和氧气的质量之和.
(3)化学反应之所以遵循质量守恒定律,从微观上看,是因为反应前后原子的种类、数目、质量均不变.
故答案为:(1)发出耀眼的白光,放出大量的热,生成一种白色固体;
(2)大于;生成氧化镁的质量等于参加反应的镁和氧气的质量之和;
(3)反应前后原子的种类、数目、质量均不变.
点评 本题难度不大,熟练掌握质量守恒定律、微观上守恒的原因并能灵活运用是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列物质中,含有氧分子的是( )
| A. | 液氧 | B. | MnO2 | C. | CO2 | D. | H2O2 |
2.原子和分子的根本区别是( )
| A. | 是否可以再分成更小的微粒 | B. | 是否保持物质的化学性质 | ||
| C. | 是否属于构成物质的微粒 | D. | 是否在化学变化中可以再分 |
19.氮肥能促使植物的茎、叶生长茂盛.某农田的农作物正值长叶期,应施下列化肥中的( )
| A. | K2SO4 | B. | CO(NH2)2 | C. | K2CO3 | D. | Ca(H2PO4)2 |
2.下列说法正确的是( )
| A. | 相对原子质量约等于质子数与电子数之和 | |
| B. | 同种元素组成的物质一定是单质 | |
| C. | 阳离子的核外电子数小于核内质子数 | |
| D. | 化学变化过程中分子数一定不会改变 |
 实验室用氯酸钾和二氧化锰的混合物制取氧气,请回答下列问题:
实验室用氯酸钾和二氧化锰的混合物制取氧气,请回答下列问题: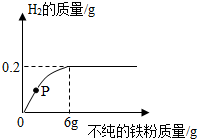 向一定量的稀盐酸中逐渐加入某种不纯的铁粉,加入铁粉的量与生成H2的关系如图所示,请回答有关问题:
向一定量的稀盐酸中逐渐加入某种不纯的铁粉,加入铁粉的量与生成H2的关系如图所示,请回答有关问题: