题目内容
6.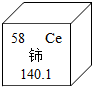 铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )
铈是一种稀土元素,在元素周期表中铈元素的某些信息如图所示,下列有关铈的说法正确的是( )| A. | 原子核内质子数为58 | B. | 属于非金属元素 | ||
| C. | 相对原子质量140.1g | D. | 原子核内中子数为58 |
分析 根据图中元素周期表可以获得的信息:左上角的数字表示原子序数;字母表示该元素的元素符号;中间的汉字表示元素名称;汉字下面的数字表示相对原子质量,进行分析判断即可.
解答 解:A.根据铈元素在元素周期表中的信息,可知铈元素的原子序数为58,则其原子核内的质子数为58,故正确;
B.根据化学元素汉字名称的偏旁可辨别元素的种类,金属元素名称一般有“金”字旁;因此铈元素属于金属元素,故错误;
C.根据相对原子质量是有单位的,其单位为“1”,因此铈元素的相对原子质量140.1,故错误;
D.根据元素周期表中的一格中获取的信息,该元素的原子序数为58;根据原子序数=核电荷数=质子数,则该元素的原子核内质子数为58,而不是核内中子数为58,故错误.
故选A.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息及辨别元素种类的方法进行分析解题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17.NO难溶于水,通常条件下极易与O2反应.则实验室收集NO的方法为( )
| A. | 向下排空气法 | B. | 向上排空气法 | C. | 排水集气法 | D. | 以上方法都可以 |
14.化学与我们生活密切相关,下列有关说法不正确的是( )
| A. | 铁制品表面生锈后,形成保护膜,会减慢锈蚀速度 | |
| B. | 洗涤剂能洗掉油污是因为洗涤剂具有乳化功能 | |
| C. | 菜刀用后立即用抹布擦干防止生锈 | |
| D. | 铝制锅盖不可以用钢刷擦洗 |
11.酸、碱、盐在工农业生产和日常生活中具有广泛的应用,下列有关其生产或应用的说法不合理的是( )
| A. | 小苏打可治疗胃酸过多,同样也可以焙制糕点 | |
| B. | 高温锻烧石灰石可制得生石灰,生石灰遇水反应生成熟石灰 | |
| C. | 利用氢氧化钠能与酸反应原理,可降低土壤的酸性 | |
| D. | 将铵态氮肥与草木灰混合施用,会增加肥效 |
15.某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)从以上数据可知,最后剩余的0.6g固体的成分是铜;这六次实中,第五次加入稀硫酸时样品中的镁已经完全反应;表格中,m=2.5.
(2)计算该过程放出气体的总质量.
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | mg |
| 第二次加入10g | 2.0g |
| 第三次加入10g | 1.5g |
| 第四次加入10g | 1.0g |
| 第五次加入10g | 0.6g |
| 第六次加入10g | 0.6g |
(2)计算该过程放出气体的总质量.
16.如图所示的四个图象,能正确反映对应变化关系的是( )
| A. |  镁在氧气中燃烧 | |
| B. |  向二氧化锰中加入过氧化氢溶液 | |
| C. |  向一定量的铁粉和铜粉的混合物中加入硫酸铜溶液 | |
| D. |  等质量的镁、铝分别与质量分数相等且足量的稀硫酸反应 |