题目内容
(2011?平房区二模)已知将氯酸钾加热到较高温度时,氯酸钾可以发生分解放出氧气.现有氯酸钾和氯化钾的固体混合物共319.5克,在较高温度下将其加热至固体质量不再减少为止.而后将所得固体加入足量的水中充分溶解后,再向其中加入足量的硝酸银溶液,充分反应后得沉淀的质量为430.5克.则原固体混合物中氯酸钾的质量分数为( )
【答案】分析:根据氯化钾和硝酸银反应的化学方程式,利用沉淀的质量可求出氯化钾的质量;根据质量守恒定律,原固体混合物的质量和氯化钾的质量之差就是氯酸钾分解放出氧气的质量;然后根据氯酸钾分解的化学方程式,利用氧气质量得到氯酸钾的质量,进而求出原固体混合物中氯酸钾的质量分数.
解答:解:设与硝酸银反应的氯化钾的质量为x
KCl+AgNO3═KNO3+AgCl↓
74.5 143.5
x 430.5g

x=223.5g
所以原固体混合物分解产生的氧气为:319.5g-223.5g=96g
设原固体混合物中氯酸钾的质量为y
2KClO3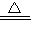 2KCl+3O2↑
2KCl+3O2↑
245 96
y 96g

y=245g
所以原固体混合物中氯酸钾的质量分数为: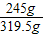 ×100%=76.7%
×100%=76.7%
故选C
点评:此题是根据化学方程式的计算题,但此题涉及的方程式较多,步骤有点复杂.一需同学们理清做题思路,二需正确写出所需的化学方程式,三计算一定要准确,有了这三点此题就能完整解出.
解答:解:设与硝酸银反应的氯化钾的质量为x
KCl+AgNO3═KNO3+AgCl↓
74.5 143.5
x 430.5g

x=223.5g
所以原固体混合物分解产生的氧气为:319.5g-223.5g=96g
设原固体混合物中氯酸钾的质量为y
2KClO3
 2KCl+3O2↑
2KCl+3O2↑ 245 96
y 96g

y=245g
所以原固体混合物中氯酸钾的质量分数为:
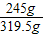 ×100%=76.7%
×100%=76.7%故选C
点评:此题是根据化学方程式的计算题,但此题涉及的方程式较多,步骤有点复杂.一需同学们理清做题思路,二需正确写出所需的化学方程式,三计算一定要准确,有了这三点此题就能完整解出.

练习册系列答案
相关题目