题目内容
6.粗盐中除NaCl外,还含有MgCl2、CaCl2以及泥沙等杂质,为了有效将粗盐提纯,实验的各步操作流程如图所示.请回答: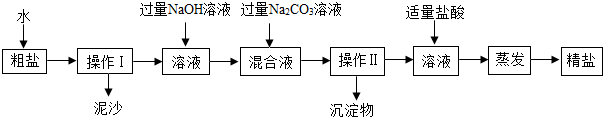
(1)操作Ⅰ和Ⅱ是相同的操作,其名称是什么?
(2)主写出加入过量的NaOH溶液时发生反应的化学方程式.
(3)加Na2CO3溶液的目的是什么?
(4)加入适量盐酸的目的是什么?
分析 (1)分离固体与溶液的方法是过滤;
(2)氢氧化钠可以将水中的镁离子转化为沉淀而得到净水的目的,书写化学方程式;
(3)根据碳酸钠与氯化钙反应进行分析;
(4)盐酸与氢氧化钠、碳酸钠反应.
解答 解:(1)分离固体与溶液的方法是过滤,I、II都是分离出沉淀的过程,所以其操作为过滤;
(2)加入过量的氢氧化钠,氢氧根离子可以和镁离子转化为氢氧化镁沉淀而将镁离子除去,化学方程式为:MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(3)加Na2CO3溶液的目的是:碳酸根离子可以和钙离子转化为碳酸钙沉淀而将钙离子除去;
(4)加入适量盐酸的目的是除掉过量的氢氧化钠和碳酸钠,得到纯净的氯化钠溶液.
点评 本题考查了物质的除杂的有关问题,难度比较大,特别的除去食盐中的多种杂质,要根据除杂的原理深入思考,按照最优化的顺序添加除杂剂.

练习册系列答案
相关题目
16.下列关于物质组成与分类的说法中,正确的是( )
| A. | 含有氧元素的化合物叫做氧化物 | |
| B. | NH3由一个氮元素和三个氢元素组成 | |
| C. | 原子核是由质子和电子构成的 | |
| D. | 氢氧化钠的构成粒子是Na+和OH- |
17.下列物质的用途中,利用其物理性质的是( )
| A. | 红磷:用作烟雾弹 | B. | 氮气:用作食品包装袋中的填充气 | ||
| C. | 干冰:用于人工降雨 | D. | 小苏打:用于治疗胃酸过多 |
1.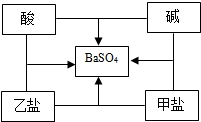 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
 小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )
小明同学在总结酸、碱、盐之间的相互反应关系时发现,选用适当物质可实现图中所示的所有反应.若中间的物质为硫酸钡,那么对酸、碱、甲盐、乙盐四种物质的推断中,合理的是( )| A. | HCl NaOH BaCl2 Na2SO4 | B. | HCl Ba(OH)2 Na2SO4 BaCl2 | ||
| C. | H2SO4 Ba(OH)2 Na2SO4 BaCl2 | D. | H2SO4 NaOH BaCl2 Na2SO4 |
11.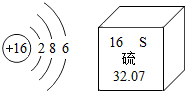 如图是硫原子的结构示意图和硫元素在元素周期表中的信息,下列说法错误的是( )
如图是硫原子的结构示意图和硫元素在元素周期表中的信息,下列说法错误的是( )
 如图是硫原子的结构示意图和硫元素在元素周期表中的信息,下列说法错误的是( )
如图是硫原子的结构示意图和硫元素在元素周期表中的信息,下列说法错误的是( )| A. | 原子的核电荷数为16 | B. | 最外层电子数为6 | ||
| C. | 属于金属元素 | D. | 相对原子质量为32.07 |
18.分离、提纯是化学实验的重要手段,下列方法中不能达到目的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | NaOH 溶液(Na2SO4) | 加入适量的Ba(OH)2溶液、过滤 |
| B | CaO(CaCO3) | 加水溶解、过滤 |
| C | O2(H2O) | 通入盛有浓硫酸的洗气瓶 |
| D | 铁粉(锌粉) | 加过量FeS04溶液充分反应后过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
15.下列鉴别物质的方法错误的是( )
| A. | 用酚酞鉴别食盐水和醋酸 | B. | 用灼烧法鉴别羊毛线与棉纱线 | ||
| C. | 用水鉴别生石灰和熟石灰 | D. | 用水鉴别氢氧化钠、硝酸铵、氯化钠 |
16.物质性质决定用途.下列说法正确的是( )
| A. | O2能支持燃烧,可作燃料 | |
| B. | 浓H2SO4有吸水性,可用于干燥氨气 | |
| C. | 新制Cu(OH)2能与葡萄糖反应,可用于糖尿病的检查 | |
| D. | 明矾溶于水能形成吸附性物质,可用于自来水的杀菌消毒 |