题目内容
18.课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数.(1)【化学方法】向11.7克氯化钠溶液中加入足量硝酸银溶液,得到2.87 克氯化银白色沉淀,则该氯化钠溶液中氯化钠的质量分数为多少?
(2)【物理方法】取一定量该氯化钠溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) | 25.0 |
| 蒸发皿+食盐溶液(g) | 45.0 |
| 蒸发皿+食盐晶体(g) | 27.4 |
| 数据处理 | 溶液中溶质的质量分数为12%. |
分析 (1)根据生成的沉淀的质量和对应的化学方程式求算氯化钠的质量,进而求算对应的质量分数;
(2)根据溶质的质量和溶液的质量求算对应的质量分数.
解答 解:
(1)设氯化钠的质量为x
NaCl+AgNO3=NaNO3+AgCl↓
58.5 143.5
x 2.87g
$\frac{58.5}{143.5}$=$\frac{x}{2.87g}$
x=1.17g
该氯化钠溶液中氯化钠的质量分数为$\frac{1.17g}{11.7g}$×100%=10%
(2)溶质的质量为27.4g-25.0g=2.4g
溶液的质量为45.0g-25.0g=20.0g
溶液中溶质的质量分数为$\frac{2.4g}{20g}$×100%=12%
故答案为:(1)10%;(2)12%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
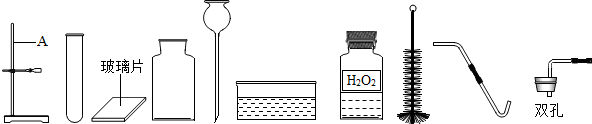
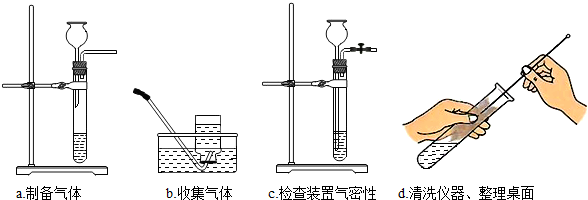
13.规范实验操作是实验成功的基础,操作不当可能会造成严重的实验结果.根据如图所示实验,对可能造成的实验结果描述错误的是( )


| A. | 集气瓶破裂 | B. | 酸液飞溅 | C. | 测定结果偏大 | D. | 收集不满O2 |
3.氢氧化钠和浓硫酸可作气体干燥剂,下列可用这两种物质干燥的是( )
①CO ②CO2 ③H2 ④SO2 ⑤O2 ⑥H2S ⑦NH3.
①CO ②CO2 ③H2 ④SO2 ⑤O2 ⑥H2S ⑦NH3.
| A. | ①③⑤ | B. | ①③⑦ | C. | ②④⑥ | D. | ③⑤⑦ |
7.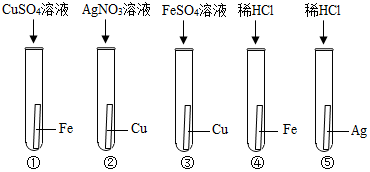 某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如图所示的实验操作,其中可以达到实验目的组合是( )
某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如图所示的实验操作,其中可以达到实验目的组合是( )
 某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如图所示的实验操作,其中可以达到实验目的组合是( )
某化学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如图所示的实验操作,其中可以达到实验目的组合是( )| A. | ①③ | B. | ②③ | C. | ②④ | D. | ④⑤ |
8.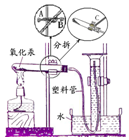 如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑,下列有关本实验的描述错误的是( )
如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑,下列有关本实验的描述错误的是( )
 如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑,下列有关本实验的描述错误的是( )
如图是研究性学习课题《化学反应中质量守恒的研究》的实验装置.本实验通过测定氧化汞分解前后反应物和生成物的质量是否相等来验证质量守恒定律.已知:氧化汞分解的反应方程式:2HgO$\frac{\underline{\;\;△\;\;}}{\;}$2Hg+O2↑,下列有关本实验的描述错误的是( )| A. | 在量筒中加入一些煤油,可以减少氧气在水中的溶解 | |
| B. | 塑料管口放出连续均匀的气泡后才能收集气体 | |
| C. | 氧化汞未分解完全就停止加热对实验结果没有影响 | |
| D. | 塑料管伸入量筒底部,可使测定氧气体积更准确 |
 截止2014年1月28日,浙江共确诊人感染H7N9禽流感病例49例.人感染H7N9禽流
截止2014年1月28日,浙江共确诊人感染H7N9禽流感病例49例.人感染H7N9禽流