题目内容
9.根据如图回答问题.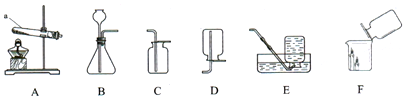
(1)仪器a的名称是试管.
(2)实验室用高锰酸钾制取氧气的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,所选用的收集装置是E或C.
(3)实验室用双氧水和二氧化锰粉末支取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,收集一瓶氧气,将带火星的木条放在集气瓶口,若观察到木条复燃,说明瓶中已充满氧气.
(4)如图F所示,将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是密度比空气的密度大,不可燃且不助燃.
分析 (1)熟记仪器的名称;
(2)熟记实验室用高锰酸钾制取氧气的化学反应式;根据气体的密度与溶解性选择收集装置;
(3)根据反应的原理、化学方程式的写法以及氧气的验满方法来分析;
(4)将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是:二氧化碳的密度比空气的密度大,二氧化碳不可燃且不助燃.
解答 解:(1)仪器a是试管;故填:试管;
(2)用加热高锰酸钾制取氧气的同时还生成锰酸钾和二氧化锰,反应的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;因氧气的密度大于空气的密度,并不易溶于水,所以可以用排水法和向上排空气法收集.故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;C;
(3)在二氧化锰的催化作用下,过氧化氢分解为水和氧气;用排空气法收集一瓶氧气,验满时将带火星的木条放在瓶口,若观察到木条复燃,说明瓶中已充满氧气;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;木条复燃;
(4)将二氧化碳倒入烧杯中,观察到燃烧的蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是:二氧化碳的密度比空气的密度大,二氧化碳不可燃且不助燃.故填:密度比空气的密度大,不可燃且不助燃.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和二氧化碳的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
19.某科学兴趣小组为了研究物质燃烧的剧烈程度与氧气浓度的关系,需要收集一瓶大约含四分之一空气的氧气,下列操作正确的是( )
| A. |  集气瓶中$\frac{1}{4}$的水 | B. |  集气瓶中灌$\frac{3}{4}$的水 | ||
| C. |  导管伸入到集气瓶体积的$\frac{1}{4}$处 | D. |  导管伸入到集气瓶体积的$\frac{3}{4}$处 |
20.下列实验现象的描述中,正确的是( )
| A. | 灼烧棉花后可以闻到一股烧焦羽毛的气味 | |
| B. | 把洁净的铜丝放入硝酸银溶液中,溶液由无色逐渐变蓝色 | |
| C. | 加热硫酸铜晶体可观察到由白色变蓝色 | |
| D. | 氢氧化钠固体和硝酸铵固体溶于水都会放出热量 |
17. 汽车给生活带来便捷也造成了环境污染.汽车尾气中含有二氧化碳、一氧化碳、二氧化硫、氮氧化物等.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )
汽车给生活带来便捷也造成了环境污染.汽车尾气中含有二氧化碳、一氧化碳、二氧化硫、氮氧化物等.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )
 汽车给生活带来便捷也造成了环境污染.汽车尾气中含有二氧化碳、一氧化碳、二氧化硫、氮氧化物等.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )
汽车给生活带来便捷也造成了环境污染.汽车尾气中含有二氧化碳、一氧化碳、二氧化硫、氮氧化物等.“三效催化转换器”可将汽车尾气中的有毒气体处理为无污染的气体.如图表示治理汽车尾气所涉及反应的微观过程.下列说法不正确的是( )| A. | 图中单质的化学式为N2 | B. | 该反应使有害气体转化为无害气体 | ||
| C. | 该反应属于置换反应 | D. | 生成单质与化合物的质量比为7:22 |
1.小明给量筒内液体读数,开始时仰视读数为25mL,倒出一部分后,俯视读数为20mL,则实际倒出的液体体积为( )
| A. | 等于5mL | B. | 小于5mL | C. | 大于5mL | D. | 无法判断 |
18.课外活动时,同学们采用以下两种方法测定某氯化钠溶液的溶质质量分数.
(1)【化学方法】向11.7克氯化钠溶液中加入足量硝酸银溶液,得到2.87 克氯化银白色沉淀,则该氯化钠溶液中氯化钠的质量分数为多少?
(2)【物理方法】取一定量该氯化钠溶液进行蒸发,测量实验数据如下:
(1)【化学方法】向11.7克氯化钠溶液中加入足量硝酸银溶液,得到2.87 克氯化银白色沉淀,则该氯化钠溶液中氯化钠的质量分数为多少?
(2)【物理方法】取一定量该氯化钠溶液进行蒸发,测量实验数据如下:
| 蒸发皿的质量(g) | 25.0 |
| 蒸发皿+食盐溶液(g) | 45.0 |
| 蒸发皿+食盐晶体(g) | 27.4 |
| 数据处理 | 溶液中溶质的质量分数为12%. |

 请根据硝酸钾、氯化铵两种固体物质的溶解度曲线回答下列问题:
请根据硝酸钾、氯化铵两种固体物质的溶解度曲线回答下列问题: