题目内容
(2010?西城区一模)了解物质构成的微观奥秘,能帮助我们更好地认识物质变化的本质.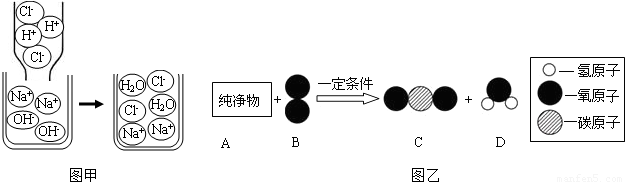
(1)氧和硅在地壳中含量丰富,两种元素的本质区别是它们原子结构中的数不同;碳(原子序数6)与硅(原子序数14)具有相似的化学性质,这主要是因为它们原子结构中的数相同.
(2)如图甲是盐酸与氢氧化钠溶液反应的微观过程示意图.
构成氢氧化钠溶液的粒子是;盐酸与氢氧化钠溶液的反应属于基本反应类型中的反应,从微观粒子的角度分析,该反应的实质是.
(3)纯净物A可用作气体燃料.在一定条件下,将一定质量的A与160g B按如图乙所示充分反应,当B反应完全时,生成132g C和72g D.
A中各元素的质量比是.已知A的相对分子质量为44,该反应的化学方程式是.
【答案】分析:(1)掌握决定元素种类的因素;化学性质由最外层电子数决定;
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子、其基本反应类型;从微观粒子的角度分析,该反应酸与碱中和的实质;
(3)由已知“将一定质量的A与160gB按下图所示充分反应,当B反应完全时,生成132gC和72gD”,根据质量守恒定律,则可求A参加反应的质量;由“132gC和72gD”,结合模型图可推测C为二氧化碳,D为水,可以求出二氧化碳中的碳元素的质量,水中氢元素的质量,即A中各元素的质量比;已知A的相对分子质量为44,该反应的化学方程式.
解答:解:(1)氧和硅在地壳中含量丰富,两种元素的本质区别是它们原子结构中的质子数不同,因为元素种类由质子数决定;碳(原子序数6)与硅(原子序数14)具有相似的化学性质,主要因为它们原子结构中的最外层电子数相同;
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子为Na+、OH-、H2O;其基本反应类型为复分解反应;从微观粒子的角度分析,该反应酸与碱中和的实质为:氢离子和氢氧根离子结合生成水分子;
(3)由已知“将一定质量的A与160gB按下图所示充分反应,当B反应完全时,生成132gC和72gD”,根据质量守恒定律,则可求A参加反应的质量为:132+72-160=44克;结合模型图可推测C为二氧化碳,D为水,则“132gC中和72gD”二氧化碳中的碳元素的质量为132× ×100%=36克,水中氢元素的质量为72×
×100%=36克,水中氢元素的质量为72× ×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2
×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2 3CO2+4H2O.
3CO2+4H2O.
故答为:(1)质子数;最外层电子数;
(2)Na+、OH-、H2O;复分解;氢离子和氢氧根离子结合生成水分子;
(3)m(C):m(H)=9:2;C3H8+5O2 3CO2+4H2O
3CO2+4H2O
点评:了解微粒观点及模型图的应用;掌握原子的有关数量计算;掌握元素质量比的计算.
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子、其基本反应类型;从微观粒子的角度分析,该反应酸与碱中和的实质;
(3)由已知“将一定质量的A与160gB按下图所示充分反应,当B反应完全时,生成132gC和72gD”,根据质量守恒定律,则可求A参加反应的质量;由“132gC和72gD”,结合模型图可推测C为二氧化碳,D为水,可以求出二氧化碳中的碳元素的质量,水中氢元素的质量,即A中各元素的质量比;已知A的相对分子质量为44,该反应的化学方程式.
解答:解:(1)氧和硅在地壳中含量丰富,两种元素的本质区别是它们原子结构中的质子数不同,因为元素种类由质子数决定;碳(原子序数6)与硅(原子序数14)具有相似的化学性质,主要因为它们原子结构中的最外层电子数相同;
(2)由盐酸与氢氧化钠溶液反应的微观过程示意图可知,构成氢氧化钠溶液的粒子为Na+、OH-、H2O;其基本反应类型为复分解反应;从微观粒子的角度分析,该反应酸与碱中和的实质为:氢离子和氢氧根离子结合生成水分子;
(3)由已知“将一定质量的A与160gB按下图所示充分反应,当B反应完全时,生成132gC和72gD”,根据质量守恒定律,则可求A参加反应的质量为:132+72-160=44克;结合模型图可推测C为二氧化碳,D为水,则“132gC中和72gD”二氧化碳中的碳元素的质量为132×
 ×100%=36克,水中氢元素的质量为72×
×100%=36克,水中氢元素的质量为72× ×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2
×100%=8克;因为碳元素、氢元素都来自A,故A中各元素的质量比m(C):m(H)=36:8=9:2;已知A的相对分子质量为44,则A的化学式为C3H8,故该反应的化学方程式是C3H8+5O2 3CO2+4H2O.
3CO2+4H2O.故答为:(1)质子数;最外层电子数;
(2)Na+、OH-、H2O;复分解;氢离子和氢氧根离子结合生成水分子;
(3)m(C):m(H)=9:2;C3H8+5O2
 3CO2+4H2O
3CO2+4H2O点评:了解微粒观点及模型图的应用;掌握原子的有关数量计算;掌握元素质量比的计算.

练习册系列答案
相关题目
(2010?西城区一模)小波在“化学氧自救器”的说明书中看到“人呼出的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气”,对自救器内发生的化学反应原理产生了探究欲望.他与同学们一起进行了实验探究活动.

活动Ⅰ:探究CO2与超氧化钾(KO2)反应确实可以生成O2.
查阅资料:超氧化钾(KO2)能与CO2、H2O反应生成O2;
未查到超氧化钾(KO2)能否与HCl气体反应的资料.
进行实验:同学们设计了如下实验装置.其中A装置的作用是除去CO2中混入的HCl气体,该反应的化学方程式是______.B装置中盛放的液体药品是______.D装置的作用是______(用化学方程式表示).为了得出结论,最后还要进行的实验操作是______.
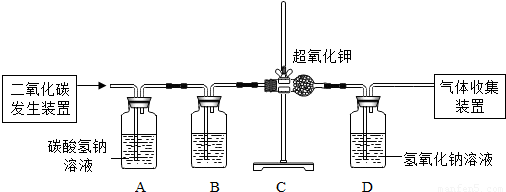
活动Ⅱ:探究二氧化碳与超氧化钾反应除生成氧气外还生成什么物质?
老师提示:二氧化碳与超氧化钾反应的产物只有氧气和某化合物.
做出猜想:二氧化碳与超氧化钾反应生成的化合物是什么?小波同学做出了三种猜
想:①是一种酸;②是一种碱;③是一种碳酸盐.
通过分析,小英同学认为猜想①和②是错误的,她得出此结论的依据是______.
进行实验:验证猜想③是正确的.
反思评价:二氧化碳与超氧化钾反应的化学方程式是______.滴加稀盐酸后,若不将产生的气体通入澄清石灰水,就不能验证猜想③是正确的,其理由是______.

活动Ⅰ:探究CO2与超氧化钾(KO2)反应确实可以生成O2.
查阅资料:超氧化钾(KO2)能与CO2、H2O反应生成O2;
未查到超氧化钾(KO2)能否与HCl气体反应的资料.
进行实验:同学们设计了如下实验装置.其中A装置的作用是除去CO2中混入的HCl气体,该反应的化学方程式是______.B装置中盛放的液体药品是______.D装置的作用是______(用化学方程式表示).为了得出结论,最后还要进行的实验操作是______.

活动Ⅱ:探究二氧化碳与超氧化钾反应除生成氧气外还生成什么物质?
老师提示:二氧化碳与超氧化钾反应的产物只有氧气和某化合物.
做出猜想:二氧化碳与超氧化钾反应生成的化合物是什么?小波同学做出了三种猜
想:①是一种酸;②是一种碱;③是一种碳酸盐.
通过分析,小英同学认为猜想①和②是错误的,她得出此结论的依据是______.
进行实验:验证猜想③是正确的.
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量二氧化碳与超氧化钾反应后的固体于试管中,滴加适量稀盐酸,并将产生的气体通入澄清石灰水中. | 固体逐渐消失,有无色气泡产生,澄清石灰水变浑浊. | 猜想③是正确的. |