题目内容
14.3.0g某有机物在足量的氧气中完全燃烧,生成8.8g二氧化碳和5.4g水,则该有机物的化学式为( )| A. | CH4 | B. | C2H6 | C. | C2H5OH | D. | CH3OH |
分析 根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素.化合物中原子的个数比=$\frac{元素的质量比}{相对原子质量比}$,可以计算出该物质分子中各原子的个数比.
解答 解:8.8gCO2中含有碳元素的质量为:8.8g×$\frac{12}{44}$×100%=2.4g,5.4g水中含有氢元素的质量为:5.4g×$\frac{1×2}{18}$×100%=0.6g,生成物8.8g二氧化碳和5.4g水中所含碳、氢元素的质量和=2.4g+0.6g=3g,则该物质中一定含有碳、氢两种元素,一定不含氧元素.
该物质的分子中碳、氢两种原子的个数比为$\frac{2.4g}{12}$:$\frac{0.6g}{1}$=2:6,则该有机物的化学式为C2H6.
故选:B.
点评 本题难度稍大,主要考查了质量守恒定律、化学式的计算,解题的关键是根据质量守恒定律确定确定物质的元素组成.

练习册系列答案
相关题目
5.下列四种微粒中,具有相似的化学性质的是( )


| A. | ②③ | B. | ①④ | C. | ②④ | D. | ①② |
4.下列物质的用途中,主要是利用其物理性质的是( )
| A. | 用氮气制尿素等化肥 | B. | 用氧气急救病人 | ||
| C. | 用干冰进行人工降雨 | D. | 用氦气、氩气做保护气 |
11.下列反应中,属于复分解反应的是( )
| A. | CO2+H2O═H2CO3 | B. | HCl+AgNO3═HNO3+AgCl↓ | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ |
8.为测定其真实的含钙量,孙东同学每次取10片钙片放入已称量的含足量盐酸的烧杯中,钙片中除CaCO3 外,其它成分不与HCl反应.充分反应后再称取烧杯和剩余物的总质量.孙东同学做了三次实验,数据如表:
请列式计算每片这样的钙片含碳酸钙的质量.
| 物质的质量 | 第一次 | 第二次 | 第三次 | 平均值 |
| 反应前;烧杯+盐酸 | 22g | 22g | 22g | 22g |
| 10片钙片 | 8g | 8g | 8g | 8g |
| 反应后;烧杯+剩余物 | 26.7g | 26.5g | 26.9g | 26.7g |
9.下列图象不能正确反映对应变化关系的是( )
| A. | 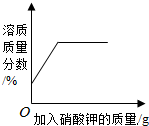 20℃时,向一定量的硝酸钾不饱和溶液中加入硝酸钾固体 | |
| B. | 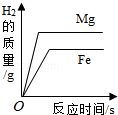 将等质量的镁片和铁片投入到足量稀硫酸中 | |
| C. | 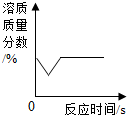 向某温度下一定量的熟石灰饱和溶液中加入少量生石灰 | |
| D. | 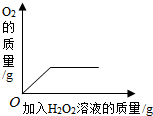 向盛有少量二氧化锰的烧杯中不断地加入过氧化氢溶液 |

