题目内容
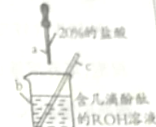 如图所示,对某碱ROH溶液100g进行中和反应实验,逐滴加入36.5g20%的盐酸时,溶液变成无色,已知ROH中R的质量分数为57.5%,问:
如图所示,对某碱ROH溶液100g进行中和反应实验,逐滴加入36.5g20%的盐酸时,溶液变成无色,已知ROH中R的质量分数为57.5%,问:(1)图中仪器名称:
a.
b.
c.
(2)实验中加入酚酞试液的作用是
(3)计算反应前ROH溶液的溶质质量分数.
考点:根据化学反应方程式的计算,常用仪器的名称和选用,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据实验室常用仪器解答;
(2)根据加入酚酞试液的作用是证明酸碱恰好完全反应;
(3)根据酸碱反应的方程式,利用盐酸的质量求出ROH溶液的溶质的质量.
(2)根据加入酚酞试液的作用是证明酸碱恰好完全反应;
(3)根据酸碱反应的方程式,利用盐酸的质量求出ROH溶液的溶质的质量.
解答:解:
(1)根据实验室常用仪器可知是:a胶头滴管;b烧杯;c玻璃棒;
(2)加入酚酞试液的作用是证明酸碱恰好完全反应;
(3)设R的相对原子质量为x
×100%=57.5%
x=25
设反应前ROH溶液的溶质的质量为y
ROH+HCl=RCl+H2O
42 36.5
y 36.5g×20%
=
y=8.4g
反应前ROH溶液的溶质质量分数为:
×100%=8.4%
答案:
(1)a胶头滴管;b烧杯;c玻璃棒;
(2)证明酸碱恰好完全反应
(3)反应前ROH溶液的溶质质量分数为8.4%.
(1)根据实验室常用仪器可知是:a胶头滴管;b烧杯;c玻璃棒;
(2)加入酚酞试液的作用是证明酸碱恰好完全反应;
(3)设R的相对原子质量为x
| x |
| x+16+1 |
x=25
设反应前ROH溶液的溶质的质量为y
ROH+HCl=RCl+H2O
42 36.5
y 36.5g×20%
| 42 |
| y |
| 36.5 |
| 36.5g×20% |
y=8.4g
反应前ROH溶液的溶质质量分数为:
| 8.4g |
| 100g |
答案:
(1)a胶头滴管;b烧杯;c玻璃棒;
(2)证明酸碱恰好完全反应
(3)反应前ROH溶液的溶质质量分数为8.4%.
点评:本题考查了根据化学方程式的计算,完成此题,可以依据已有的溶液和化学方程式计算的知识进行.

练习册系列答案
相关题目
下列实验现象描述正确的是( )
| A、红磷在空气中燃烧产生大量烟雾 |
| B、铁丝在空气中燃烧后生成黑色固体 |
| C、硫在氧气中燃烧发出蓝紫色火焰 |
| D、电解水实验中负极产生气体和正极产生气体的体积比为1:2 |
将甲、乙、丙三种金属分别放入稀硫酸中,只有甲产生气泡,将乙、丙放入硫酸铜溶液中,丙表面析出红色金属,乙没有明显现象.据此判断,三种金属的金属活动性顺序是( )
| A、甲>乙>丙 |
| B、乙>丙>甲 |
| C、丙>甲>乙 |
| D、甲>丙>乙 |