题目内容
12.在AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色.有关判断正确的是( )| A. | 滤渣中一定有Ag,没有Cu和Zn | |
| B. | 滤渣中一定有Ag和Zn,可能有Cu | |
| C. | 滤液中一定有Zn(NO3)2、Cu(NO3)2,可能有AgNO3 | |
| D. | 滤液中一定有Zn(NO3)2、Cu(NO3)2、AgNO3 |
分析 根据金属银、铜、锌的活动性由强到弱的顺序锌>铜>银,当把锌粉加入到AgNO3和Cu(NO3)2的混合溶液中,首先置换出银,银被置换完才继续置换铜.
解答 解:金属银、铜、锌的活动性由强到弱的顺序锌>铜>银,当把锌粉加入到AgNO3和Cu(NO3)2的混合溶液中,首先置换出银,银被置换完才继续置换铜.
在AgNO3、Cu(NO3)2的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色,说明溶液中一定含有硝酸铜,锌会与硝酸银发生反应,所以溶液中一定含有硝酸锌,无法确定加入锌的质量,所以硝酸银可能完全反应,也可能部分反应;硝酸铜可能部分反应,所以
A、滤渣中一定有Ag,可能有Cu,一定没有锌,故A错误;
B、滤渣中一定有Ag,可能有Cu,一定没有锌,故B错误;
C、滤液中一定有Zn(NO3)2、Cu(NO3)2,可能有AgNO3,故C正确;
D、滤液中一定有Zn(NO3)2、Cu(NO3)2,可能有AgNO3,故D错误.
故选:C.
点评 本题考查的是金属和盐溶液的反应,把金属放入多种盐的混合溶液中,首先把活动性最弱的金属置换出来,置换的先后顺序为由弱到强,最强的最后置换出来.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
13.学习小组的同学进行下列有关氧气的实验,其中相应实验装置有错误的是( )
| A. |  空气中氧气含量的测定 | B. |  氧气的制取 | ||
| C. |  氧气的干燥 | D. |  铁丝在氧气中燃烧 |
3.人类利用金属矿物历史久远.
(1)现代冶炼技术用CO与赤铁矿石反应来冶炼生铁,请写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:
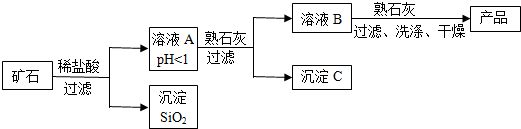
①溶液A中共含有4种阳离子;
②在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为是6.7≤pH<8.6;
③溶液B中一定含有的溶质为MgCl2、CaCl2(填化学式).
(1)现代冶炼技术用CO与赤铁矿石反应来冶炼生铁,请写出该反应的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)某矿石由MgO、Fe2O3、CuO和SiO2组成,用它制备氢氧化镁的流程示意图如图所示:

①溶液A中共含有4种阳离子;
②在溶液A中加入熟石灰调节溶液的pH,可以使溶液中的金属阳离子转化为沉淀,该实验条件下,使金属阳离子沉淀的相关pH数据见下表.为保证产品纯度、减少产品损失,并便于操作,溶液B的pH可允许的范围为是6.7≤pH<8.6;
| 氢氧化物 | Fe(OH)3 | Cu(OH)2 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 4.2 | 8.6 |
| 完全沉淀的pH | 3.2 | 6.7 | 11.1 |
20.安徽是农业大省,水稻是安徽省的主要粮食作物之一.下列有关水稻种植过程及其相关应用的叙述中涉及到化学变化的是( )
| A. |  栽种秧苗 | B. |  收割水稻 | C. |  稻谷晾晒 | D. |  稻草发电 |
7.下列符号与其叙述对应一致的是( )
| A. | 3H-3个氢元素 | B. | $\stackrel{+3}{Fe}$-铁元素的化合价显+3价 | ||
| C. | C60-60个碳原子 | D. | NaCO3-碳酸钠 |
17.铝合金、氧化铝、硫酸铝三种物质的分类正确的是( )
| A. | 混合物、氧化物、盐 | B. | 混合物、盐、化合物 | ||
| C. | 单质、混合物、盐 | D. | 金属单质、氧化物、纯净物 |
4.买来的榴莲放在桌子上还没有吃,满屋尽是榴莲味,这一现象说明( )
| A. | 分子很大 | B. | 分子分裂成原子 | ||
| C. | 分子间有间隔 | D. | 分子总在不断运动 |
2.某课外活动兴趣小组的同学为了测定某地区石灰石样品种碳酸钙的质量分数,取该样品16g,现将90mL稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如表:
试求:
(1)m的值是2.2g;
(2)求该样品中碳酸钙的质量分数(保留一位小数).
| 实验 | 第一次 | 第二次 | 第三次 |
| 加入稀盐酸的量/mL | 30 | 30 | 30 |
| 生成气体的质量/g | 2.2 | m | 1.1 |
(1)m的值是2.2g;
(2)求该样品中碳酸钙的质量分数(保留一位小数).
 向盛有100g不饱和Na2CO3溶液的烧杯中,滴入一定量的BaCl2溶液至恰好完全反应,然后过滤,将得到的固体物质放入烧杯中,并向其中逐滴滴入溶质质量分数为10%的稀盐酸,烧杯中难溶物质的质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答下列问题:
向盛有100g不饱和Na2CO3溶液的烧杯中,滴入一定量的BaCl2溶液至恰好完全反应,然后过滤,将得到的固体物质放入烧杯中,并向其中逐滴滴入溶质质量分数为10%的稀盐酸,烧杯中难溶物质的质量与所滴入稀盐酸的质量关系曲线如图所示.请根据题意回答下列问题: