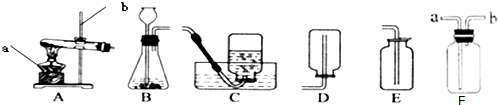
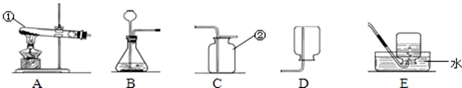
题目内容
被称为“绿色氧化剂”的过氧化氢(H2O2),俗称双氧水,是一种无色液体,常用作氧化剂、消毒杀菌剂和漂白剂等.在较低温度下和少量催化剂(如MnO2)条件下,它能迅速分解,生成氧气和水.请回答下列问题:
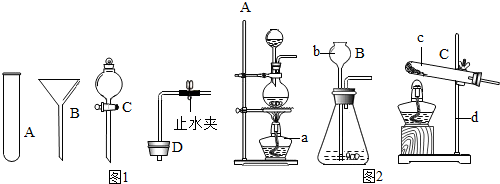
(1)写出如图1标号仪器的名称:
A ,B ,C ,D .
(2)若实验室用过氧化氢代替氯酸钾制取氧气,可采用如图2哪种发生装置? (填序号),主要理由是 .
(3)当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图1的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是 (填序号),它更换原装置中的 .控制反应速度的原理是: .
(4)天然气、沼气的主要成分是甲烷(CH4),它是无色无味的气体,密度比空气小,极难溶于水,能燃烧.实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体.若用此法制取甲烷气体,其气体发生装置选择 ,(从图2、B、C中选择)可采用 或 收集.

(1)写出如图1标号仪器的名称:
A
(2)若实验室用过氧化氢代替氯酸钾制取氧气,可采用如图2哪种发生装置?
(3)当过氧化氢接触二氧化锰后,反应便立即开始并不能人为控制其速度.如果稍改变你所选择的装置,便可控制其反应的速度.请从图1的仪器中选择一种仪器更换你选择的装置中的一种仪器,以达到控制反应速度的目的.你选择的仪器是 (填序号),它更换原装置中的
(4)天然气、沼气的主要成分是甲烷(CH4),它是无色无味的气体,密度比空气小,极难溶于水,能燃烧.实验室用无水醋酸钠和碱石灰固体混合物加热制取甲烷气体.若用此法制取甲烷气体,其气体发生装置选择
考点:氧气的制取装置,氧气的收集方法
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟悉常见仪器,了解它们的名称;
(2)分解过氧化氢制取氧气,是在常温下的反应,据此选择发生装置;
(3)要控制反应的速度可以用分液漏斗代替长颈漏斗,因为分液漏斗可使液体的滴加随开随停;
(4)根据此反应是固体和固体的加热反应,选择发生装置;再根据它的密度比空气小,极难溶于水,选择收集装置.
(2)分解过氧化氢制取氧气,是在常温下的反应,据此选择发生装置;
(3)要控制反应的速度可以用分液漏斗代替长颈漏斗,因为分液漏斗可使液体的滴加随开随停;
(4)根据此反应是固体和固体的加热反应,选择发生装置;再根据它的密度比空气小,极难溶于水,选择收集装置.
解答:解:(1)熟悉常见仪器,了解它们的名称.仪器分别是:酒精灯、长颈漏斗、试管、铁架台.
故答案为:酒精灯、长颈漏斗、试管、铁架台;
(2)用过氧化氢制取氧气,要用二氧化锰做催化剂,在常温下反应,所以要用装置B.
故答案为:B;过氧化氢在常温下(不需要加热)可以分解生成氧气;
(3)图中的分液漏斗可以使液体的滴加随开随停,从而控制反应的速度,所以要控制反应的速度,我们可用图中C代替原装置中的长颈漏斗;
故答案为:C、b、分液漏斗可以使液体的滴加随开随停;
(4)甲烷的制取是用无水醋酸钠和碱石灰的固体混合物加热制取的.也就是固体和固体的加热反应,属于“固体加热型”,所以可用装置C作为发生装置;因为甲烷的密度比空气小,极难溶于水,可用排水法和向下排空气法收集.
故答案为:C、排水法或向下排空气法(两点顺序可颠倒).
故答案为:酒精灯、长颈漏斗、试管、铁架台;
(2)用过氧化氢制取氧气,要用二氧化锰做催化剂,在常温下反应,所以要用装置B.
故答案为:B;过氧化氢在常温下(不需要加热)可以分解生成氧气;
(3)图中的分液漏斗可以使液体的滴加随开随停,从而控制反应的速度,所以要控制反应的速度,我们可用图中C代替原装置中的长颈漏斗;
故答案为:C、b、分液漏斗可以使液体的滴加随开随停;
(4)甲烷的制取是用无水醋酸钠和碱石灰的固体混合物加热制取的.也就是固体和固体的加热反应,属于“固体加热型”,所以可用装置C作为发生装置;因为甲烷的密度比空气小,极难溶于水,可用排水法和向下排空气法收集.
故答案为:C、排水法或向下排空气法(两点顺序可颠倒).
点评:本题主要考查实验装置的选取,以及实验仪器等知识,这就要求我们熟悉实验选择装置的依据及仪器的用途.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列诗句中不含有化学变化的是( )
| A、爆竹声中一岁除,春风送暖入屠苏 |
| B、野火烧不尽,春风吹又生 |
| C、日照香炉生紫烟,遥看瀑布挂前川 |
| D、春蚕到死丝方尽,蜡炬成灰泪始干 |
下列有关氧气的叙述正确的是( )
| A、氧气能支持燃烧,可作燃料 |
| B、鱼能在水中生存,说明氧气易溶于水 |
| C、氧气在空气中的质量分数为21% |
| D、氧气能和大多数物质反应,说明氧气的化学性质比较活泼 |
下列四个图象中,能正确表示化学反应中对应的变化关系的是( )
A、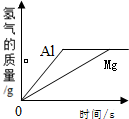 向两份等质量的相同稀硫酸中加入足量的镁粉和铝粉 |
B、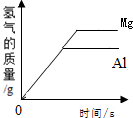 向等质量的镁粉、铝粉中分别滴加足量相同的稀硫酸 |
C、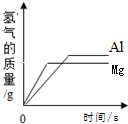 向等质量的镁粉、铝粉中分别加入足量相同的稀硫酸 |
D、 用等质量等浓度的双氧水分别制取氧气 |
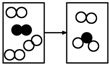 如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子.
如图是密闭体系中某反应的微观示意图,“○”和“●”分别表示不同原子. B.
B. C.
C.
 构成的物质生成的化学反应方程式
构成的物质生成的化学反应方程式