题目内容
8.下列说法正确的是( )| A. | 碳-12原子和碳-13原子的中子数相同 | |
| B. | KMnO4和K2MnO4中有相同的原子团 | |
| C. | Fe2+和Fe3+都属于铁元素,核外电子数不同 | |
| D. |  和 和 化学性质相同 化学性质相同 |
分析 A、根据碳-12原子和碳-13原子的区别分析;
B、根据KMnO4和K2MnO4中含有的原子团不同分析;
C、根据这两个微粒所表示的意义分析;
D、根据不同元素的化学性质不同分析;
解答 解:A、碳-12原子中有6中子,碳-13原子中有7中子,故错误;
B、KMnO4中的原子团是高锰酸根,在化合物中的化合价为-1价;而K2MnO4中的原子团是锰酸根,在化合物中的化合价为-2价,种类不同,故错误;
C、它们都属于铁元素,但核外电子数不同,Fe2+的核外电子数比核内质子数少2个,Fe3+的核外电子数比核内质子数少3个,故正确;
D、 和
和 的核内质子数不同,不是同种元素,最外层易得失电子的状况不同,化学性质不同,故错误;
的核内质子数不同,不是同种元素,最外层易得失电子的状况不同,化学性质不同,故错误;
故选:C
点评 本题涉及到的知识点较多,有原子和离子的相互转化,核外电子在化学反应中的作用,元素的概念,化合价的表示等.解题的关键是要知道离子和原子之间的联系,化合价和离子所带电荷之间的关系.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.2017年4月,天舟一号与天宫二号成功完成推进剂在轨补加任务.偏二甲肼(C2H8N2)可用作推动火箭发射的燃料,下列有关其说法正确的是( )
| A. | 偏二甲肼的相对分子质量为60 | |
| B. | 偏二甲肼中碳、氮元素的质量比为1比l | |
| C. | 偏二甲肼中氢元素质量分数最大 | |
| D. | 偏二甲肼分子由C2H8分子和N2分子构成 |
19.你认为下列观点不正确的是( )
| A. | 物质本身并无优劣之分,但应用的方法和目的却存在好与坏的差别 | |
| B. | “低碳”理念是为了引导全社会把二氧化碳的排放量设法控制在合理的范围内 | |
| C. | 随着仿真实验室和数字处理技术的发展,研究的结论可不必通过实验来证明 | |
| D. | 化学变化中所说的“新物质”就是在组成或结构上与变化前不同的物质 |
13.下列所示的四个图象,能正确反映对应变化关系的是( )
| A. |  电解水 | |
| B. |  向两份完全相同的稀盐酸中分别加入锌粉和铁粉 | |
| C. |  加热一定质量的高锰酸钾 | |
| D. |  向一定量的氢氧化钠溶液中加水稀释 |
20.下列有关化学实验操作的图示中不正确的是( )
| A. |  检查气密性 | B. |  熄灭酒精灯 | C. |  吸取液体 | D. |  滴加液体 |
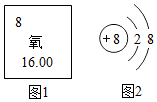 如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.
如图1是氧元素在元素周期表中的相关信息,图2是该元素形成的一种粒子的结构示意图.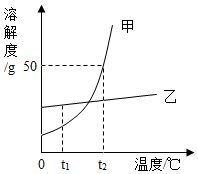 如图为甲和乙两种固体物质的溶解度曲线.回答下列问题:
如图为甲和乙两种固体物质的溶解度曲线.回答下列问题: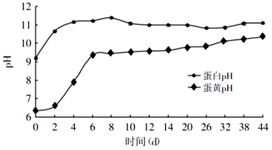 阅读下面科普短文(本文由网络文章改写).
阅读下面科普短文(本文由网络文章改写).