题目内容
如图是探究空气中氧的含量的装置图.
(1)实验前要检查 .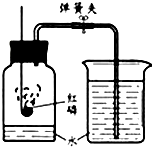
(2)红磷燃烧,你观察到的现象是 ;化学反应的方程式: .
(3)打开弹簧夹,观察到 ,说明空气中氧气约占空气总体积的
.
(4)通过此实验还可得出集气瓶内剩余气体(即氮气)具有的性质 .(写一点)
(5)实验过程中往往会出现测量值偏小的情况,可能的原因有: (写一点)
(1)实验前要检查

(2)红磷燃烧,你观察到的现象是
(3)打开弹簧夹,观察到
| 1 |
| 5 |
(4)通过此实验还可得出集气瓶内剩余气体(即氮气)具有的性质
(5)实验过程中往往会出现测量值偏小的情况,可能的原因有:
考点:空气组成的测定,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:根据测定空气中氧气的含量的实验步骤、注意事项分析.(1)装置的气密性必须是良好的,红磷的量是过量的,等装置冷却后再打开弹簧夹.(2)根据红磷燃烧的反应写出反应的方程式;
(3)根据瓶内压强的变化及空气中氧气的体积分数分析.(4)根据实验中的现象分析剩余的气体具有的性质(5)根据实验的注意事项分析;
(3)根据瓶内压强的变化及空气中氧气的体积分数分析.(4)根据实验中的现象分析剩余的气体具有的性质(5)根据实验的注意事项分析;
解答:解:(1)该实验必须检查装置的气密性,若装漏气,所测的结果不准确;
(2)红磷燃烧时产生大量的白烟,集气瓶内充满白烟,红磷燃烧生成了五氧化二磷,反应的方程式是:4P+5O2
2P2O5;
(3)由红磷燃烧生成了五氧化二磷固体,瓶内压强减少,打开弹簧夹后,水由烧杯流向集气瓶,流入集气瓶中水的体积应该是集气瓶空间体积的
左右.
(4)实验中瓶中的氧气被消耗,依据实验中氧气耗尽后红磷不能继续燃烧,且打开止水夹后水进入到集气瓶中与剩余固体共存可知剩余气体具有以下性质:不燃烧也不支持燃烧,不易溶于水;
(5)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.都会使进入的水少于五分之一.
故答案为:(1)装置的气密性;(2)产生大量的白烟;4P+5O2
2P2O5;(3)水由烧杯流向集气瓶,流入集气瓶中水的体积应该是集气瓶空间体积的
;(4)不燃烧也不支持燃烧,不易溶于水(5)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.
(2)红磷燃烧时产生大量的白烟,集气瓶内充满白烟,红磷燃烧生成了五氧化二磷,反应的方程式是:4P+5O2
| ||
(3)由红磷燃烧生成了五氧化二磷固体,瓶内压强减少,打开弹簧夹后,水由烧杯流向集气瓶,流入集气瓶中水的体积应该是集气瓶空间体积的
| 1 |
| 5 |
(4)实验中瓶中的氧气被消耗,依据实验中氧气耗尽后红磷不能继续燃烧,且打开止水夹后水进入到集气瓶中与剩余固体共存可知剩余气体具有以下性质:不燃烧也不支持燃烧,不易溶于水;
(5)①红磷的量不足,使瓶内氧气未耗尽 ②瓶塞未塞紧,使外界空气进入瓶内 ③未冷却至室温就打开止水夹,使进入瓶内水的体积减少 ④烧杯中的水不够等.都会使进入的水少于五分之一.
故答案为:(1)装置的气密性;(2)产生大量的白烟;4P+5O2
| ||
| 1 |
| 5 |
点评:只有全面地掌握了实验室测定空气中氧气含量的实验的原理、步骤及注意事项才能完成有关的问题.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
下列说法中,你认为不正确的是( )
| A、氢的原子核中没有中子 |
| B、氢原子的核外只有一个电子 |
| C、氢原子失去电子以后就是一个质子 |
| D、若某原子的最外层上只有一个电子,该原子一定是氢原子 |
类推是化学学习中常用的思维方法,以下备选答案不正确的是 ( )
①碱的水溶性显碱性,所以碱性溶液一定是碱的溶液②碳酸盐与盐酸反应生产气体,所以与盐酸生成气体的一定是碳酸盐.③有机物都含碳元素,所以含碳元素的一定是有机物.④化学反应往往伴随则发光、放热,产生气体,生成沉淀或颜色的改变等明显现象.如果没有看到明显现象,说明没有发生化学变化.⑤酸碱中和生成盐和水,所以生成盐和水的反应是中和反应.
①碱的水溶性显碱性,所以碱性溶液一定是碱的溶液②碳酸盐与盐酸反应生产气体,所以与盐酸生成气体的一定是碳酸盐.③有机物都含碳元素,所以含碳元素的一定是有机物.④化学反应往往伴随则发光、放热,产生气体,生成沉淀或颜色的改变等明显现象.如果没有看到明显现象,说明没有发生化学变化.⑤酸碱中和生成盐和水,所以生成盐和水的反应是中和反应.
| A、只有①②③④ |
| B、只有①②④⑤ |
| C、只有②③④⑤ |
| D、①②③④⑤ |
下列用数轴表示的化学知识,正确的是( )
A、空气质量级别与空气质量状况的关系: |
B、地壳中部分元素的含量关系: |
C、部分元素原子序数关系: |
D、空气中部分成分的体积分数关系: |
如图所示实验不能达到目的是( )
A、 检验试管中的固体物质中含有碳酸根 检验试管中的固体物质中含有碳酸根 |
B、 探究物质燃烧的条件 探究物质燃烧的条件 |
C、 本组实验可证明凸透镜对光线有会聚作用 |
D、 压缩乙醚蒸气可使其液化 压缩乙醚蒸气可使其液化 |