题目内容
5.2015年3月20日联合国发布报告,到2030年,全球将有40%的国家和地区面临干旱问题,节约用水和合理开发利用水资源是每个公民应尽的责任和义务.下列关于水的认识正确的是( )| A. | 过滤能将硬水软化 | |
| B. | 活性炭可以除去天然水中不溶性杂质 | |
| C. | 工业污水要先达标后排放 | |
| D. | 生活污水直接排放不会造成水体污染 |
分析 A、根据过滤是把不溶于液体的固体与液体分离的一种方法,进行分析判断.
B、根据活性炭具有吸附性,进行分析判断.
C、根据工业废水中含有有毒、有害物质,进行分析判断.
D、根据生活污水直接排放会造成水体污染进行分析判断.
解答 解:A、过滤能除去天然水中的难溶性杂质,但不能除去可溶性的钙镁化合物,不能将硬水软化,故选项说法错误.
B、活性炭具有吸附性,能吸附异味和色素,但不能除去天然水中不溶性杂质,故选项说法错误.
C、工业废水中含有有毒、有害物质,需要处理达标后再排放,故选项说法正确.
D、生活污水直接排放会造成水体污染,故选项说法错误.
故选:C.
点评 本题难度不大,了解水体污染的来源与防治措施、硬水软化的方法等是正确解答本题的关键.

练习册系列答案
相关题目
20.甲同学在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2与二氧化碳相似,能与氢氧化钠反应.
(3)点燃充满氢气的小试管,会有轻微的爆鸣声.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
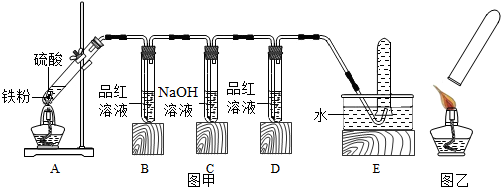
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.
请帮助小明完成如表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫.
【反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】实验结束后甲同学先撤去了酒精灯,请你预测会发生什么后果引起倒吸现象,B中液体会倒吸入A,A处热试管有可能炸裂.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$ Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2与二氧化碳相似,能与氢氧化钠反应.
(3)点燃充满氢气的小试管,会有轻微的爆鸣声.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助小明完成如表:
| A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 不褪色 | 无爆鸣声 | 只有SO2 | |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | SO2、H2都有 |
| 实验三 | 25% | 不褪色 | 只有H2 | ||
【反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】实验结束后甲同学先撤去了酒精灯,请你预测会发生什么后果引起倒吸现象,B中液体会倒吸入A,A处热试管有可能炸裂.
1.下列化学方程式符合题意且书写正确的是( )
| A. | 医疗上用碱性物质中和胃酸过多:NaOH+HCl═NaCl+H2O | |
| B. | 证明铜的活动性比银强:Cu+2AgCl═CuCl2+2Ag | |
| C. | 实验室制取氧气:2KClO3═2KCl+3O2↑ | |
| D. | 工业上用纯碱制烧碱:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH |
5.在FeO、Fe2O3、Fe3O4三种化合物中,与等质量铁相结合的氧的质量比是( )
| A. | 1:3:4 | B. | 6:9:8 | C. | 6:8:9 | D. | 6:1:4 |
17.潜艇内的氧气再生设备主要为氧气再生药板,“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na2O2),过氧化钠使用后变成白色固体.现对白色固体的成分进行探究:
【查阅资料】2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
【提出猜想】根据人体呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:
猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
【得出结论】猜想Ⅲ成立.
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
【查阅资料】2Na2O2+2CO2═2Na2CO3+O2 2Na2O2+2H2O═4NaOH+O2↑
【提出猜想】根据人体呼出的气体中含有较多的二氧化碳和水蒸气.对白色固体作出如下猜想:
猜想Ⅰ:氢氧化钠 猜想Ⅱ:碳酸钠 猜想Ⅲ:氢氧化钠和碳酸钠
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入适量氯化钙溶液; | 产生白色沉淀; | 该反应的化学方程式为Na2CO3+CaCl2=2NaCl+CaCO3↓; |
| (2)将上述反应后的混合物过滤,取滤液加入无色酚酞试液. | 无色变红色. | 证明猜想Ⅲ正确 |
【拓展应用】“氧气再生剂”的保存方法是密封存放干燥处.
14.金属M和AgNO3溶液反应的化学方程式为:M+2AgNO3═M(NO3)2+2Ag.则下列说法错误的是( )
| A. | 这个反应属于置换反应 | |
| B. | 金属M可能是铜 | |
| C. | 用M可以回收硝酸银废液中的银 | |
| D. | 反应前后元素M和N化合价发生了变化 |
15.在实验室中,为了探究金属与盐溶液的反应规律,将一定质量的锌粉放入AgNO3与Cu(NO3)2的混合溶液中,实验过程及现象如图所示,结合实际现象判断,以下结论中错误的是( )

| A. | 溶液中一定没有铜离子 | B. | 滤渣中一定含有铜、银 | ||
| C. | 滤渣中可能含有金属锌 | D. | 滤液中主要的溶质含有Zn(NO3)2 |